
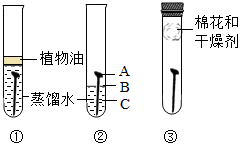
 某学习小组用相同的光亮铁钉探究铁生锈与哪些因素有关,设计的实验如图所示:
某学习小组用相同的光亮铁钉探究铁生锈与哪些因素有关,设计的实验如图所示:分析 (1)A.根据铁生锈的条件进行分析判断;B.根据试管①中蒸馏水的作用分析判断;C.根据氢氧化钠固体的物理性质进行分析判断;D.根据探究铁生锈条件的实验原理进行分析判断;
(2)根据稀盐酸的用途书写化学方程式.
解答 解:(1)A.由实验图可知试管①中铁钉缺少氧气,所以无明显现象;试管③中的铁钉缺少水份,所以无明显现象;只有试管②中的铁钉既与空气接触又与水份接触所以能生锈,而且B处铁钉与水份接触较充分所以生锈最严重,故A不正确;
B.试管①中蒸馏水的作用是隔绝空气,所以要用新制的蒸馏水,因为水在加热沸腾时水中溶解的氧气已排出,故B正确;
C.氢氧化钠固体易潮解能吸收空气中的水蒸气,成以可用于除去空气中的水蒸气,故C正确;
D.该实验可得出的结论是铁生锈需要与空气(氧气)和水份同时接触才能生锈,由此可以推断,保持铁制品表面干燥或隔绝空气和水份都可以防止钢铁生锈,故D正确;
(2)稀盐酸可以和氧化铁反应生成氯化铁和水,发生反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;
故答案为:(1)BCD;(2)Fe2O3+6HCl=2FeCl3+3H2O;
点评 此题考查学生对钢铁锈蚀条件探究实验的掌握情况,掌握铁锈蚀的条件(铁与氧气、水同时接触)并能灵活运用是正确解答本题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
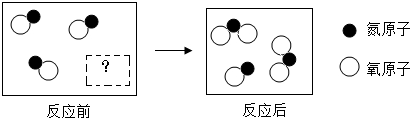
| A. | 反应前虚框中的微粒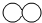 为 为 | |
| B. | 该反应过程中氮元素的化合价发生了改变 | |
| C. | 反应前后分子和原子的种类不变 | |
| D. | 该反应过程中参加反应的和生成的各分子个数比可以为2:1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
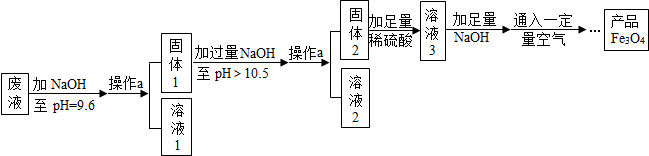
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
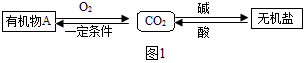
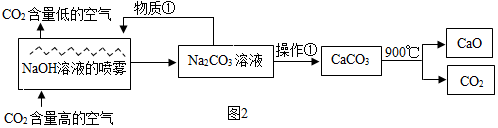
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
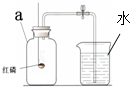 如图是小张同学测定空气中氧气体积分数的实验装置,根据题意回答以下问题.
如图是小张同学测定空气中氧气体积分数的实验装置,根据题意回答以下问题. 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com