
| 编号 | 实验I | 实验II | 实验III |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
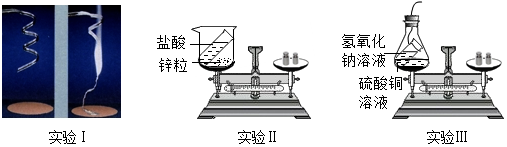
分析 (1)实验I镁条燃烧,镁条与空气中的氧气发生化合反应生成白色固体氧化镁;反应前所称量为金属镁的质量,反应后所称量的质量为金属氧化物氧化镁的质量;
(2)根据镁条与空气中的氧气发生化合反应生成白色固体氧化镁;
(3)反应前后质量之所以守恒,是由于化学变化是一个“分子破裂成原子,原子重新组合成分子”的过程,此过程中,原子种类、原子个数、原子的质量都不改变;
(4)质量守恒是指参加反应的物质的总质量不变,而实验I在反应前没有测定参加反应氧气的质量,实验II没有称量放出气体质量的质量,因此,不能说明反应前后质量不变.
解答 解:(1)根据质量守恒定律,生成的白色固体氧化镁的质量应为参加反应的镁的质量与参加反应的氧气的质量总和;而反应前所称量的质量只是金属镁的质量,而反应后称量的则是金属氧化物氧化镁的质量,所以才出现了反应后固体质量“增加”的现象;
故答案为:根据质量守恒定律,参加反应的镁带和氧气的质量总和,等于反应后生成的氧化镁的质量,由于空气中的氧气参与了反应,因此,生成氧化镁的质量比原来镁带的质量增加了;
(2)镁条与空气中的氧气发生化合反应生成白色固体氧化镁,反应的化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(3)化学变化是一个“分子破裂成原子,原子重新组合成分子”的过程,此过程中,原子种类、原子个数、原子的质量都不改变,所以,化学变化前后虽然物质发生了改变,但构成物质(分子)的原子既不减少也不改变,变化前后总质量不变;
故答案为:化学反应前后原子的种类、数目和质量没有发生改变;
(4)可把实验I中的镁条放在一密闭的容器进行点燃,称量点燃前后容器内物质的总质量,以说明质量守恒;可把实验II放在密闭容器内放出,使得产生的氢气不能逸出,以称量反应前后的总质量;
故答案为:实验I应将镁条放在密闭的金属容器中引燃,再称量(实验II使用密闭容器使产生的气体不能逸出,再进行称量).
答案:
(1)根据质量守恒定律,参加反应的镁带和氧气的质量总和,等于反应后生成的氧化镁的质量,由于空气中的氧气参与了反应,因此,生成氧化镁的质量比原来镁带的质量增加了;
(2)2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(3)化学反应前后原子的种类、数目和质量没有发生改变;
(4)实验I应将镁条放在密闭的金属容器中引燃,再称量(实验II使用密闭容器使产生的气体不能逸出,再进行称量).
点评 验证质量守恒定律时,有气体参加的实验必须密封,若不密封因气体质量的影响而造成所得的生成物的质量与反应物的质量不相等,不能得出质量守恒的结论.


科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀. | |
步骤2:取适量滤液于试管中,滴加稀硫酸. | 有①生成,说明有Ba2+. |
| 步骤3:取适量步骤1中的沉淀于试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中. | 试管中有②产生,烧杯中 ③,结合步骤2说明沉淀是BaCO3. |
| 步骤4:取适量滤液于试管中,滴加④. | 试管中有蓝色沉淀生成,说明滤液中有大量的OH-,综合上面步骤可知试剂由大量Ba(OH)2和少量BaCO3组成,假设成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuSO4 BaCl2 H2SO4 | B. | Na2CO3 Ca(NO3)2 HCl | ||
| C. | Na2SO4 KNO3 HCl | D. | MgCl2 NaOH KNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com