

分析 (1)根据包装袋上所要求的食用和储存方法,可以推测碘酸钾可能的化学性质;
(2)根据相对分子质量=各原子的相对原子质量×原子个数之和,进行分析解答;
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(4)根据化合物中元素的质量分数的计算方法进行分析解答;
(5)根据题意,由原来每千克食盐含碘30mg下调至25mg,化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答;
解答 (1)根据包装袋上所要求的食用和储存方法,可以推测碘酸钾可能的化学性质受热易分解;故填:受热易分解;
(2)碘酸钾的相对分子质量=127+39+16×3=39+127+48=214;故填:214;
(3)碘酸钾中钾元素、碘元素、氧元素的质量比为127:39:(16×3)=39:127:48.故填:39:127:48;
(4)碘酸钾中碘元素的质量分数为碘元素的质量分数$\frac{127}{214}$×100%≈59.3%.故填:59.3%;
(5)根据题意,由原来每千克食盐含碘30mg下调至25mg,加碘食盐每袋应比调整前碘元素的质量减少了(30mg-25mg)÷2=2.5mg,则每千克食用盐中少加了2.5mg×2÷59.3%≈8.4mg.故填:8.4.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
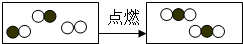 如图形象地表示了某化学反应的微观示意图,其中○表示一个氧原子,●表示一个碳原子,该反应中下列说法正确的是( )
如图形象地表示了某化学反应的微观示意图,其中○表示一个氧原子,●表示一个碳原子,该反应中下列说法正确的是( )| A. | 反应物都是化合物 | |
| B. | 反应后分子种类不变 | |
| C. | 该反应的化学方程式可表示为CO+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | |
| D. | 该示意图说明化学反应的实质是分子分割成原子,原子再重新组合成新分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 淀粉、二氧化碳都含有碳元素,它们都属于有机物 | |
| B. | 氧气能供能呼吸,能支持燃烧,能作燃料,用途广泛 | |
| C. | 根据固体溶解度曲线图,可以知道固体的溶解度受温度的影响情况 | |
| D. | 配制100g20%的硝酸钾溶液需要称得20g硝酸钾和量取100mL水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇分子的结构模型如图所示,则下列叙述正确的是( )
农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇分子的结构模型如图所示,则下列叙述正确的是( )| A. | 乙醇是氧化物 | B. | 一个乙醇分子共有26个质子 | ||
| C. | 乙醇中碳、氧元素的质量比为3:4 | D. | 乙醇中氧元素的质量分数最大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水分子之间有间隔 | B. | 水分子在不断运动 | ||
| C. | 面粉颗粒本身运动导致 | D. | 水分子之间有作用力 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com