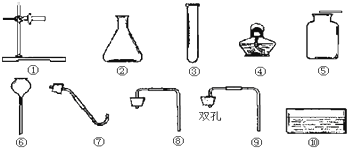
下图是实验室常用的制取气体的发生装置和收集装置.
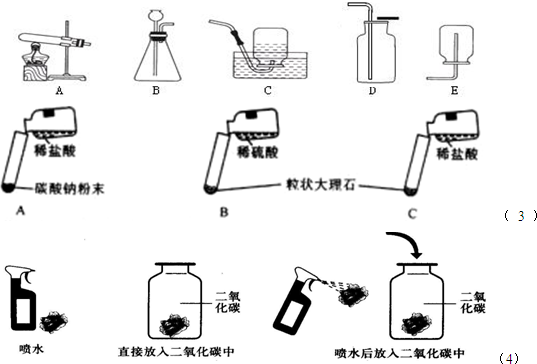
(1)实验室用A装置制取氧气的化学方程式是
,实验室用B装置制取氧气的化学方程式是
.
(2)实验室常用块状固体硫化亚铁(FeS)和稀硫酸在常温下制取硫化氢气体,有关化学方程式为:FeS+H
2SO
4=H
2S↑+FeSO
4,硫化氢气体是一种有臭鸡蛋气味的有毒的气体,能溶于水,根据上述信息回答:实验室制取硫化氢的发生装置为
B
B
(用字母序号填空),收集装置为
D
D
(用字母序号填空).
(3)某实验小组的同学用碳酸钠粉末、粒状大理石、稀盐酸、浓盐酸、稀硫酸这几种药品,探究哪两种药品的反应适合在实验室制取CO
2.请你参与下列的探究并回答问题.
【提出问题】上述酸和碳酸盐的反应是否适合在实验室制取CO
2?
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO
2,你认为原因是
浓盐酸具有挥发性
浓盐酸具有挥发性
.
讨论后大家设计了如下三个实验进行对比分析.
【实验与结论】
| 实验 |
实验现象 |
实验内容 |
| A |
剧烈反应,迅速放出大量气泡 |
反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B |
产生气泡,速率迅速减慢,反应几乎停止. |
无法持续产生CO2,不能用于实验室制取CO2 |
| C |
产生气泡,速率适中 |
速率适中持续产生CO2,能用于实验室制取CO2 |
根据探究结论,实验室制取二氧化碳选择第C组药品,该药品制取二氧化碳的反应原理为
CaCO3+2HCl=CaCl2+CO2↑+H2O
CaCO3+2HCl=CaCl2+CO2↑+H2O
( 用化学方程式表示);验满方法是
用一根燃烧的木条,平放在集气瓶口,观察木条是否熄灭
用一根燃烧的木条,平放在集气瓶口,观察木条是否熄灭
; 检验方法二氧化碳的是
倒入澄清的石灰水振荡,观察是否变浑浊
倒入澄清的石灰水振荡,观察是否变浑浊
.
【拓展与迁移】
由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:
是否连续产生气体等
是否连续产生气体等
.
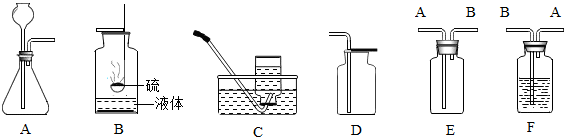
(4)如图:为了探究二氧化碳能否与水反应,现取用三朵紫色石蕊染成的干花(石蕊是一种色素,它遇酸变成红色)进行实验.
现象:第一朵紫色干花喷上水,紫花不变色;第二朵紫色干花直接放入盛满二氧化碳的集气瓶中,紫花也不变色;第三朵紫色干花先喷上水,再放入盛二氧化碳的集气瓶中,紫花
变红色
变红色
(填写关于颜色的现象).
结论:以上实验现象说明:
二氧化碳能与水反应
二氧化碳能与水反应
.反应的化学方程式是:
CO2+H2O=H2CO3
CO2+H2O=H2CO3
.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案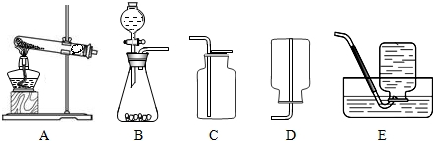

 A来制取氧气,写出该反应的化学方程式
A来制取氧气,写出该反应的化学方程式