
【题目】锌是人体生长发育、维持器官正常功能的微量元素,人体缺锌会引起多种疾病,因此缺锌者可通过服用葡萄糖酸锌等保健品来补锌。已知葡萄糖酸锌的化学式为C12H22O14Zn(相对分子质量为455)。请回答:
(1)葡萄糖酸锌由_____组成,1个葡萄糖酸锌分子中含有_____个原子;
(2)葡萄糖酸锌中所含锌元素的质量分数为_____;(保留一位小数)
(3)现有一支20mL的葡萄糖酸锌口服液,其中含锌6.5mg,则这支口服液中葡萄糖酸锌的质量为_____mg。(保留一位小数)
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:初中化学 来源: 题型:
【题目】如图中的①、②分别是钠元素、;氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图.
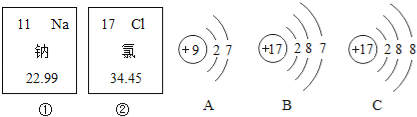
试回答下列问题:
(1)钠元素的原子序数为 ,画出它的原子结构示意图 ;
(2)A、B、C中属于同种元素的粒子是 ;
(3)A和B两种粒子的相同,所以它们具有相似的化学性质 ;
(4)钠原子和氯原子反应所形成的化合物是由 (填“分子”、“原子”、“离子”)构成的.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小丽对家中的家用制氧机产生了浓厚的兴趣。她通过阅读说明书了解到家用制氧机的工作原理如下:
(加压时,装填在制氧机内部的分子筛吸附空气中的氮气,制取高浓度氧气。减压时,分子筛将所吸附的氮气排放。整个过程中,分子筛并不消耗。)
小丽用这台家用制氧机制取并收集了一袋气体,带到实验室对其进行研究。
实验I:小丽欲通过以下实验验证所收集的气体是否为纯净的氧气。
(实验记录)
实验步骤 | 实验现象 | 文字或化学式表达式 |
取一只250 mL的集气瓶,用排水法收集一瓶所带气体,然后把一小块燃着的木炭插入集气瓶中 | 木炭燃烧得更旺 | 表达式1 |
表中,表达式1是_____。
(实验结论)收集的气体是纯净的氧气。
(实验反思)老师指出上述实验并不能证明小丽所带来的气体一定是纯净的氧气。该实验不能证明所收集气体为纯净氧气的原因是_____。
实验II:测定小丽所带气体中氧气的含量。
同学们在老师的指导下设计了如下图所示装置,进行实验,并重复多次。
 (250 mL 集气瓶)
(250 mL 集气瓶)
(实验记录)
实验操作 | 主要实验现象 | 实验结论及解释 | |
① | 检查装置的气密性 | 装置的气密性良好 | |
② | 加入药品,将装置连接固定 | ||
③ | 打开止水夹a和b,向A中缓慢鼓入一定量气体后关闭止水夹a和b | A中水进入到B中,B中水的体积为200 mL。 | 收集200 mL气体(由压强差引起的误差忽略不计) |
④ | 用凸透镜聚光引燃白磷 | 现象1 | |
⑤ | 待白磷熄灭并冷却到室温, 打开止水夹b | 现象2 | 小丽收集的气体不是纯净的氧气 |
表中,现象1是_____;现象2是_____。
(数据记录)
实验次序 | 1 | 2 | 3 | 4 | 5 |
B中剩余水体积/mL | 100 | 42 | 39 | 41 | 38 |
(数据处理)已知,在上表数据中,第1组数据偏差较大,存在明显误差,在数据处理时应删去。小丽所带气体中氧气的体积分数为_____% 。(取平均值)
(实验反思)
(1)这台家用制氧机制氧气的过程发生的变化属于_____(填“物理变化”或“化学变化”)。
(2)导致第1组数据产生较大误差的可能原因是_____。
(3)气体压力传感器可用于检测密闭体系内的气压变化,并以数字、图像等多种形式形象地显示出来。某同学用压力传感器测出实验过程中集气瓶内气压-时间关系如图2所示。
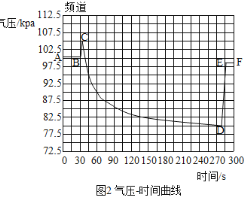
问:①图2中BC段气压变化的原因是_____;
②导致DE段气压变化的实验操作是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室现有氯酸钾、二氧化锰、石灰石、蜡烛、火柴及以下仪器(如图),请回答:
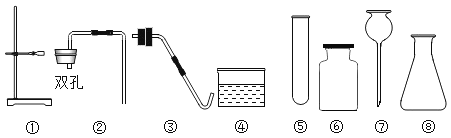
(1)仪器⑦的名称是____________;
(2)若补充一种常见仪器,并利用上述部分仪器和药品可制取一种气体,该反应的化学方程式是_______________。
(3)若补充一种药品,还能制取二氧化碳,并探究其性质(如图)
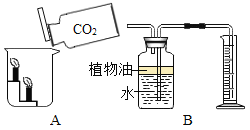
①补充的药品是_________________;
②图A观察到的现象说明二氧化碳具有的化学性质是______________;B中可用来测量生成二氧化碳气体的体积,其中在水面上放一层植物油的原因是______。
(4)2018年4月28日某媒体题为“排污工程施工,毒气放倒三人”的报道,引起某兴趣小组同学的思考。
(提出问题)排污管道中的毒气有什么成分?
(查阅资料)
I.排污管道中的大部分有机物在一定条件下发酵会产生CO、CO2、H2S、CH4等。
II.H2S气体能与CuSO4溶液反应生成黑色沉淀。
(提出猜想)小组同学对排污管道气含有上述气体中最少3种成分的猜想如下:
猜想1:有CO、CO2、H2S; 猜想2:有CO、CO2、CH4;
猜想3:有CO、H2S、CH4; 猜想4:有CO、CO2、H2S、CH4。
(实验方案)小组同学共同设计了如图所示的装置并进行探究(夹持仪器已省略)。
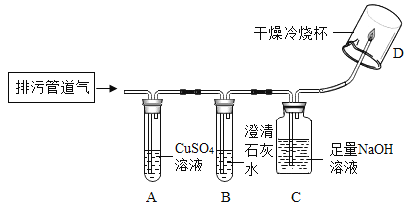
(问题讨论)
①如果A装置没有明显变化,则猜想__________成立;如果B装置没有明显变化,则猜想_________成立。
②要确证猜想4中是否有CH4,某同学认为图示装置有不足之处,需要在装置C与D之间加一个____________装置。改进后,若气体燃烧,且D装置内壁出现__________,证明气体中一定含有CH4。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用的干燥剂有浓硫酸、碱石灰(CaO和NaOH的固体混合物)等,后者在潮湿的空气中易变质。某化学兴趣小组对实验室中一瓶久置的碱石灰展开探究。
[查阅资料]①碱石灰易吸收空气中的水蒸气和二氧化碳 ②氯化钙溶液呈中性,碳酸钠溶液呈碱性 ③碳酸钠和氢氧化钙溶于水温度变化不明显 ④Ca(OH)2分解温度为580℃,CaCO3分解温度为825℃,Na2CO3的分解温度为1744℃。
[提出问题]碱石灰是否变质?其成分可能有哪些?
[进行猜想]①若没有变质,碱石灰吸水性良好,成分只有CaO和NaOH;
②若变质,该碱石灰中可能含有CaO、NaOH、Ca(OH)2、Na2CO3、CaCO3中的两种或两种以上。
[实验过程]
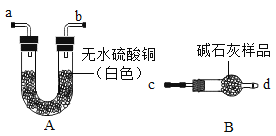
(1)验证碱石灰是否变质:图中的B为干燥装置,常用于固体干燥剂干燥气体。现用A、B装置检验碱石灰是否变质,取适量的无水硫酸铜和碱石灰样品分别装入A、B中,连接好A、B装置,从 ____(填“c”或“d”)端向B中缓缓通入水蒸气,观察A装置中的现象为____,证明碱石灰已变质。
(2)验证碱石灰是否完全变质:取适量碱石灰样品放入试管中,加入足量蒸馏水使其充分溶解,溶液变浑浊,用手触摸试管外壁,温度无明显变化,证明碱石灰已完全变质。则样品成分最多有___种可能性(填数字)。
(3)为进一步确定碱石灰样品的成分,该小组继续实验并记录如下:
实验编号 | 实验操作 | 实验目的、现象或数据 | 实验结论 |
实验一 | ①取适量样品于试管中,加入足量蒸馏水使其充分溶解; ②过滤,得到滤渣A和滤液B;③向滤液B中加入足量CaCl2溶液,静置; ④________。 | 操作③的主要目的是:___ 操作④的现象:____ | 样品中一定有Ca(OH)2 |
实验二 | ①取干燥样品50g,控制在600℃内,加热至质量不再发生变化,冷却后称量; ②将①中剩余固体控制在850℃内反复加热,冷却后称量。 | 操作①中称得固体质量为45.5g;操作②固体质量无变化。 | 样品中一定没有_____(填化学式) |
[探究结论] 通过整个探究活动分析得知碱石灰样品的成分是______(填化学式),其中盐的质量分数为_____。
[反思与评价] 通过探究活动,大家知道该碱石灰变质的化学反应过程,其中生成盐的化学方程式为______;明白了碱石灰要密封保存的原因。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硅酸钠(Na2SiO3)是我国优先发展的精细化学品。用某种石英砂矿石(主要成分是SiO2,还含有少量的CuO、Na2SO4、Na2CO3)制备硅酸钠(Na2SiO3)的流程如下:
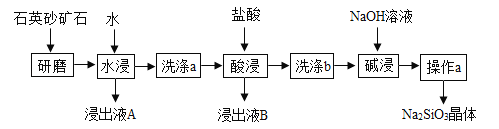
资料:SiO2既不溶于水,也不与盐酸反应。
请问答下列问题:
(1)“研磨”的目的是_______ 。
(2)检验“洗涤a”已洗净的方法是____________。
(3)“酸浸”的化学方程式为____________。
(4)“碱浸”的化学方程式为____________。
(5)“操作a”包含蒸发浓缩、_____ 、过滤、洗涤、干燥等一系列操作。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】托盘天平和量筒都属于计量仪器,已知氢氧化钠具有强烈的腐蚀性,请回答下列问题:
(1)托盘天平只能用于粗略的称量物体的质量,一般能精确到___________。
(2)要准确称取![]() 氢氧化钠,调节天平平衡时,若指针向左偏就开始称量,其他操作都正确,则称得的氢氧化钠的质量会____________(填“偏大”“偏小”或“无影响”)。
氢氧化钠,调节天平平衡时,若指针向左偏就开始称量,其他操作都正确,则称得的氢氧化钠的质量会____________(填“偏大”“偏小”或“无影响”)。
(3)小明按如图所示的操作称量![]() 氢氧化钠,他出现的错误是__________________________(答两点)。
氢氧化钠,他出现的错误是__________________________(答两点)。
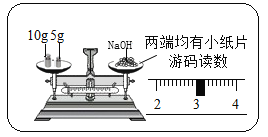
(4)量取![]() 的水,选用
的水,选用![]() 的量筒,而不选择
的量筒,而不选择![]() 的量筒,这样做的目的是_______________,量液时,该同学俯视量筒的刻度线(其他操作无误),则所量取水的体积__________(填“偏大”“偏小”或“无影响”)。
的量筒,这样做的目的是_______________,量液时,该同学俯视量筒的刻度线(其他操作无误),则所量取水的体积__________(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用过氧化氢溶液和二氧化锰(催化剂)制取氧气.
(提出问题)二氧化锰是催化剂,二氧化锰的用量对反应速率是否有影响?
(设计实验)(1)实验装置如图所示.
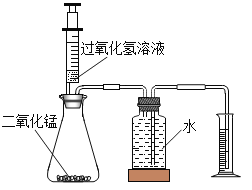
(2)实验记录:每次用30毫升10%的过氧化氢溶液,采用不同量二氧化锰粉末作催化剂进行实验,测定相关数据记录于下表中:
实验序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
二氧化锰用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
待测数据 |
(分析)(1)上述实验应该测定的“待测数据”可能是_____________.
(2)10次实验“每次用30毫升10%的过氧化氢溶液”的目的是_____________.
p>(3)若第2次实验比第3次试验的“待测数据”更______________(填“大”或“小”),说明催化剂的用量越多,反应越快.(实验与结果)经多次实验证明,第1次实验至第7次实验中过氧化氢的分解速率依次加快,第7次实验至第10次实验所记录的“待测数据”无明显差异.
(结论)__________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com