
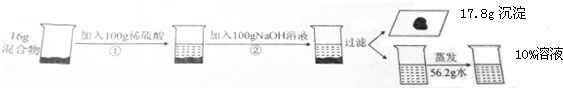
分析 (1)根据稀硫酸和氧化铜反应生成硫酸铜和水进行分析;
(2)根据质量守恒定律和生成硫酸钠的质量进行计算;
(3)根据计算出的氧化铜和铜的质量计算铜元素和氧元素的质量比;
(4)根据氢氧化钠和硫酸铜反应生成硫酸钠和氢氧化铜沉淀进行分析;
(5)根据氧化铜和硫酸反应的方程式,以及氧化铜的质量进行计算.
解答 解:(1)稀硫酸和氧化铜反应生成硫酸铜和水,化学方程式为:CuO+H2SO4=CuSO4+H2O;
(2)生成硫酸钠溶液的质量为:16g+100g+100g-17.8g-56.2g=142g,
依据硫酸根离子守恒可知,
设参加反应的氧化铜的质量为x
CuO--CuSO4----Na2SO4,
80 142
x 142g×10%
$\frac{80}{x}$=$\frac{142}{142g×10%}$
x=8g
(3)通过计算可知混合物中氧化铜质量为8g,铜的质量为8g,
所以铜元素和氧元素的质量比是:(8g+8g$\frac{64}{80}$):(8g×$\frac{16}{80}$)=9:1;
(4)通过分析可知,开始滴加氢氧化钠之前,溶质是硫酸铜,随着氢氧化钠的加入,硫酸铜质量逐渐减少,硫酸钠质量逐渐增多,最后全部转化成硫酸钠;
(5)设参加反应的硫酸钠质量为y
CuO+H2SO4=CuSO4+H2O
80 98
8g y
$\frac{80}{8g}$=$\frac{98}{y}$
y=9.8g
所以硫酸的质量分数为:$\frac{9.8g}{100g}$×100%=9.8%.
故答案为:(1)CuO+H2SO4=CuSO4+H2O;
(2)$\frac{80}{x}$=$\frac{142}{142g×10%}$;
(3)9:1;
(4)开始滴加氢氧化钠之前,溶质是硫酸铜,随着氢氧化钠的加入,硫酸铜质量逐渐减少,硫酸钠质量逐渐增多,最后全部转化成硫酸钠;
(5)9.8%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.


科目:初中化学 来源: 题型:多选题
| A. | 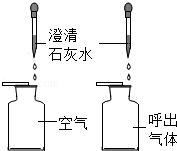 人呼出的气体中CO2含量高于空气 | B. | 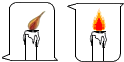 燃烧需要可燃物 | ||
| C. | 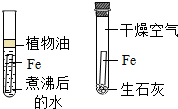 铁生锈需要氧气和水 | D. | 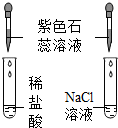 氢离子使石蕊试液变红 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
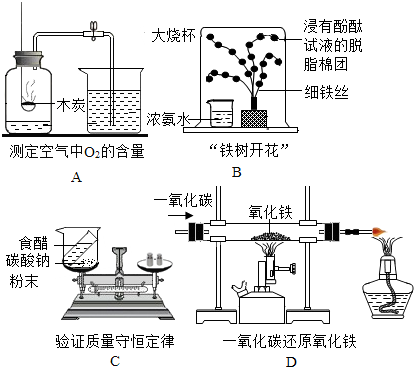
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
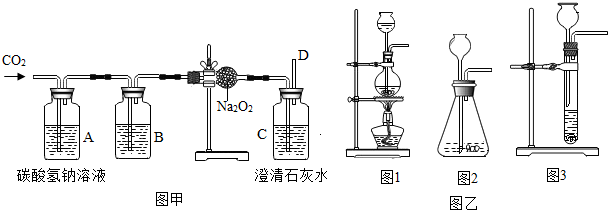
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③④⑤ | C. | ①②④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 大于10% | B. | 小于10% | C. | 等于10% | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ”表示一个氮原子,则“
”表示一个氮原子,则“ ”表示N2(填化学符号).
”表示N2(填化学符号).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
实验步骤 | 实验现象与结论 |
| ①取少量白色固体于试管中,加水振荡至全部溶解 | 无色溶液 |
| ②用pH试纸测①溶液的pH值 | 溶液的pH>7,说明氢氧化钠固体没有变质 |
实验步骤 | 实验现象与结论 |
| ①取少量白色固体于试管中,加水进行振荡至全部溶解 | 无色溶液 |
| ②向①溶液中加入适量氯化钡溶液 | 产生白色沉淀,说明氢氧化钠固 体已变质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com