
【题目】镁带在二氧化碳中燃烧的化学方程式为2Mg+CO2点燃2MgO+C,该反应属于
A. 分解反应 B. 化合反应 C. 复分解反应 D. 置换反应
科目:初中化学 来源: 题型:
【题目】下列实验现象描述不正确的是
A. 氢氧化钠溶液中滴加硫酸铜溶液产生蓝色沉淀
B. 铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体
C. 铵盐与碱溶液混合加热,产生的气体使湿润的蓝色石蕊试纸变红
D. 镁条和稀盐酸反应产生大量气泡,试管外壁发烫
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是NaCl、MgSO4、KCl固体的溶解度曲线,下列说法正确的是( )
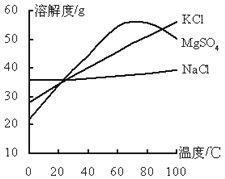
A. 60℃时三种物质的饱和溶液中,溶质质量分数最大的是KCl溶液
B. 将80℃不饱和的MgSO4溶液降温至40℃,一定能得到其饱和溶液
C. 40℃时MgSO4的溶解度比NaCl小
D. 将80℃含有少量NaCl的KCl饱和溶液降温至20℃,可得到KCl晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】公园里部分植物的枝叶枯黄,茎也比较纤细。建议工作人员施用的一种复合肥是
A. NH4HCO3 B. KNO3 C. Ca(H2PO4)2 D. KCl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸镁水合物是制备镁产品的中间体。
【制取MgCO3·3H2O】工业上从弱碱性卤水(主要成分为MgCl2)中获取MgCO3·3H2O的方法如下:

图1 获取MgCO3·3H2O的工艺流程
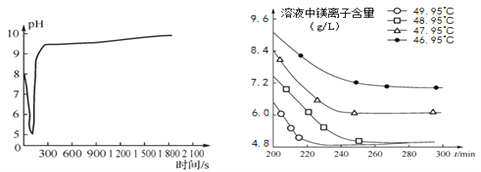
图2 沉淀过程的pH变化 图3 不同温度下溶液中镁离子含量随时间的变化
(1)沉淀过程的化学方程式为:
MgCl2+CO2+2NaOH+2H2O![]() MgCO3·3H2O↓+2_________。
MgCO3·3H2O↓+2_________。
(2)沉淀过程的pH随时间的变化如图2所示,沉淀过程的操作为_______(填字母)。
a. 向卤水中滴加NaOH溶液,同时通入CO2
b. 向NaOH溶液中滴加卤水,同时通入CO2
c. 向卤水中通入CO2至饱和,然后滴加NaOH溶液,同时继续通入CO2
d. 向NaOH溶液中通入CO2至饱和,然后滴加卤水,同时继续通入CO2
(3)沉淀过程的溶液中镁离子含量随时间的变化如图3所示,不同温度下所得到沉淀产物如表所示。
不同反应温度下的水合碳酸镁
温度(℃) | 产物 |
46.95 | MgCO3·3H2O |
47.95 | MgCO3·3H2O |
48.95 | MgCO3·3H2O |
49.95 | Mg5(OH)2(CO3)4·4H2O |
则沉淀过程选择的温度为_________,理由是_________。
【测定MgCO3·3H2O的纯度】
利用下图所示装置(图中夹持仪器略去)进行实验,以确定MgCO3·3H2O的纯度。
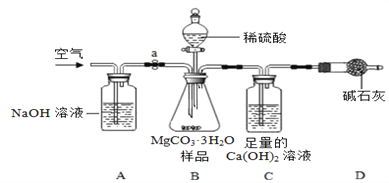
依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气,其作用除了可搅拌B、C中的反应物外,还有_________。
(2)C中反应生成CaCO3的化学方程式为___________;D中碱石灰的作用为___________。
(3)下列各项措施中,不能提高测定准确度的是___________(填标号)。
a.在加入硫酸之前,应排净装置内的CO2气体
b.为了缩短实验时间,快速滴加硫酸
c.在A~B之间增添盛有浓硫酸的洗气装置
d.在C装置左侧导管末端增添多孔球泡
(4)实验中准确称取15.0 g样品三份,进行三次测定,测得中生成CaCO3沉淀的平均质量为10.0 g。请计算样品中MgCO3·3H2O的纯度(写出计算过程)。 ______________________
(5)小明认为应将澄清石灰水换成Ba(OH)2溶液,其理由除了Ba(OH)2溶解度大,浓度大,使CO2被吸收的更完全外,还有___________。
(6)若获取MgCO3·3H2O的样品中含有少量Mg5(OH)2(CO3)4·4H2O,则产品中镁元素的质量分数_______(填“偏大”“不变”或“偏小”,下同),样品中MgCO3·3H2O的纯度_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生产生活中不可缺少的物质.下列关于水的说法中,不合理的是( )
A. 用淘米的水浇花可节约水资源
B. 通过化学变化可以直接将水转变为汽油
C. 水在催化剂和太阳能的共同作用下可分解获得氢能
D. 浓硫酸沾上皮肤,必须先用大量水冲洗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com