
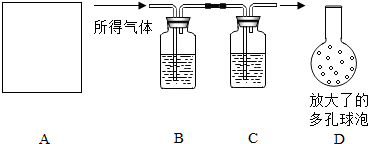
 为了测定某石灰石矿样的纯度(其中所含杂质不与酸反应),某同学按如下流程进行实验:用盐酸溶解矿样→干燥所得气体→用NaOH溶液吸收气体→根据NaOH溶液的增重量计算矿样的纯度.实验过程中所取矿样的质量为10g.实验装置如图所示:
为了测定某石灰石矿样的纯度(其中所含杂质不与酸反应),某同学按如下流程进行实验:用盐酸溶解矿样→干燥所得气体→用NaOH溶液吸收气体→根据NaOH溶液的增重量计算矿样的纯度.实验过程中所取矿样的质量为10g.实验装置如图所示:分析 (1)根据为了完成溶解至少还需要的实验仪器是什么,须知此实验共须哪些仪器进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(3)根据浓硫酸具有吸水性,可做干燥剂进行分析;
(4)根据实验须注意的事项进行分析;
(5)根据将插入溶液的管子的下端改成具有多孔的球泡后可以增大气体与溶液的接触面积,使气体被充分吸收进行分析;
(6)根据C瓶中多出的质量是吸收生成的CO2的质量,以及CaCO3+2HCl=CaCl2+H2O+CO2↑可计算出CaCO3的质量,根据碳酸钙的质量分数=$\frac{碳酸钙的质量}{样品总质量}$可计算出其质量分数.
解答 解:(1)要完成此实验,需要的实验仪器有长颈漏斗、双孔橡胶塞、导气管、广口瓶(或锥形瓶、大试管、烧瓶),所以至少还需要的实验仪器是:广口瓶(或锥形瓶、大试管、烧瓶);
(2)石灰石的化学式是CaCO3,盐酸的化学式为HCl,故A中发生的反应是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)浓硫酸具有吸水性,可做干燥剂,所以B中所盛的试剂是浓硫酸;
(4)①实验开始A、B装置以及导气管内残留有少量空气,这样溶液使实验不精确,不能正确计算反应物的生成;
②说明在前面的反应过程中没有完全反应;
③气体通过速度过快,CO2来不及被NaOH溶液全部吸收,会使计算结果不准确;
④实验结束时,系统内还残留有少量CO2气体,说明CO2没有被NaOH溶液全部吸收,会使计算结果不准确;
故选:①②③④;
(5)多孔的球泡可以增大气体与溶液的接触面积,使气体被充分吸收,有利于提高实验的准确度.故答案为:可以增大气体与溶液的接触面积,使气体被充分吸收;
(6)设样品中CaCO3的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.6g
$\frac{100}{x}$=$\frac{44}{3.6g}$
x≈8.2g
样品中CaCO3的质量分数为:$\frac{8.2g}{10g}$×100%=82%.
故答案为:(1)广口瓶(或锥形瓶、大试管、烧瓶);
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)浓硫酸;
(4)①②③④;
(5)可以增大气体与溶液的接触面积,使气体被充分吸收;
(6)样品中CaCO3的质量分数为82%.
点评 本题主要测试学生对实验操作的掌握和物质纯度的计算,学生必须牢记操作实验步骤和注意事项,并能熟练运用质量分数公式进行计算,才能正确解答.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 工业上采用分离液态空气法制氧气,该原理是利用氮气和氧气的密度不同进行分离 | |
| B. | 实验室制取气体的原料必须是纯净物 | |
| C. | 可燃物的着火点属于其本身固有的性质,一般难以改变 | |
| D. | 污染空气的主要有害气体有包括二氧化硫、一氧化碳、二氧化氮和臭氧四种氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学老师指导某化学兴趣小组,测定鸡蛋壳的主要成分碳酸钙的质量分数.他们将1:2的盐酸加入到l2g鸡蛋壳中,产生二氧化碳气体的情况如图所示.(假设鸡蛋壳中的其它成分不与盐酸发生反应)
化学老师指导某化学兴趣小组,测定鸡蛋壳的主要成分碳酸钙的质量分数.他们将1:2的盐酸加入到l2g鸡蛋壳中,产生二氧化碳气体的情况如图所示.(假设鸡蛋壳中的其它成分不与盐酸发生反应)查看答案和解析>>
科目:初中化学 来源: 题型:推断题
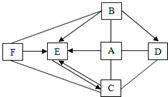 A、B、C、D、E、F及甲、乙均为初中化学常见物质,请回答下列问题:
A、B、C、D、E、F及甲、乙均为初中化学常见物质,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
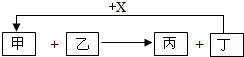
| 甲 | 乙 | 丁 | X | |
| A | 化合物 | 化合物 | 单质 | 单质 |
| B | 酸 | 碱 | 氧化物 | 氧化物 |
| C | 盐 | 碱 | 碱 | 氧化物 |
| D | 金属 | 盐 | 盐 | 碱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
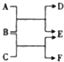 如图所示,A~F是初中化学常见的物质,已知E是氧化物中相对分子质量最小的物质,C与D反应可产生气体,试回答下列问题:
如图所示,A~F是初中化学常见的物质,已知E是氧化物中相对分子质量最小的物质,C与D反应可产生气体,试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com