
分析 (1)根据质量守恒定律可以判断物质的化学式,
(2)根据化学方程式计算参加反应的二氧化氯和水的质量比.
(3)根据题意分析.
解答 解:(1)由2ClO2+H2O═HClO2+X可知,反应前后原子个数不变,反应物中有2个Cl原子,5个O原子,2个H原子,生成物中有1个Cl原子,2个O原子,1个H原子,故每个X中含有1个Cl原子,3个O原子,1个H原子,化学式为HClO3.故填:HClO3;
(2)根据2ClO2+H2O═HClO2+HClO3,可知,
135 18
所以参加反应的二氧化氯和水的质量比为135:18=15:2.
(3)根据“二氧化氯见光易分解,”可得:见光易分解,根据“且能与水反应:2ClO2+H2O═HClO2+X”可得:与水反应.故填:与水反应或见光易分解.
点评 本题考查质量守恒定律和化学方程式的应用,难度不大,根据已有知识分析.


科目:初中化学 来源: 题型:填空题
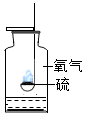 用如图所示的装置实验时,集气瓶底部预先装有少量水,它的作用是吸收二氧化硫,防止污染空气,
用如图所示的装置实验时,集气瓶底部预先装有少量水,它的作用是吸收二氧化硫,防止污染空气,查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某同学利用如图所示装置探究水的组成,通电前先在水中加入少量的硫酸或氢氧化钠,目的是:增强水的导电性.通电一段时间后,观察到的现象是均产生气泡,且生成的气体体积不同,与电源负极相连的试管内汇集的气体较多,试管2内产生的气体是氧气,正极和负极产生气体的体积比约是1:2,通过该实验可得到的结论是水是由氢元素和氧元素组成的.水通电的符号(化学式)表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
某同学利用如图所示装置探究水的组成,通电前先在水中加入少量的硫酸或氢氧化钠,目的是:增强水的导电性.通电一段时间后,观察到的现象是均产生气泡,且生成的气体体积不同,与电源负极相连的试管内汇集的气体较多,试管2内产生的气体是氧气,正极和负极产生气体的体积比约是1:2,通过该实验可得到的结论是水是由氢元素和氧元素组成的.水通电的符号(化学式)表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
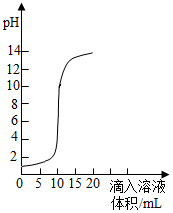 右图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
右图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化钙:CaO2 | B. | 碳酸钠:Na2CO3 | C. | 硫酸铝:AlSO4 | D. | 氯化铁:FeCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②③①④⑥⑤ | B. | ③②①④⑤⑥ | C. | ③②①④⑥⑤ | D. | ②③①④⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com