
| 在不同pH溶液中浸泡后 | |||||
| pH=1 | pH=4 | pH=7 | pH=10 | pH=13 | |
| 头发光泽 | 无明显变化 | 无明显变化 | 无明显变化 | 黄 | 黄、无光泽 |
| 头发拉断难易程度 | 不易断 | 不易断 | 不易断 | 易断 | 极脆 |
分析 由题目的信息可知:测定溶液的pH时,为了使测定结果更准确,往往需要多做几次实验,然后取其平均值.根据实验结果可知,pH为1~7时,头发的光泽都没有明显的变化,且都不易断,说明酸性溶液对头发影响不大;而当pH=10时,头发发黄,且易折断,pH再增大为13时,头发无光泽,且极脆,说明碱性溶液对头发影响较大,且碱性越强对头发影响越大.不同人头发的主要成分是相同的,故得到的结论应该是一样的.洗发时先用洗发液再用护发素;因为洗发液显碱性,洗去头发上的油污,护发素显酸性,中和洗发液的碱性,保护头发.
解答 解:
测定溶液的pH时,为了使测定结果更准确,往往需要多做几次实验,然后取其平均值,故答案为:提高测定pH的准确性(或减小实验误差);
【实验结论】.
根据实验结果可知,pH为1~7时,头发的光泽都没有明显的变化,且都不易断,说明酸性溶液对头发影响不大;而当pH=10时,头发发黄,且易折断,pH再增大为13时,头发无光泽,且极脆,说明碱性溶液对头发影响较大,且碱性越强对头发影响越大,故答案为:碱性溶液对头发影响大,酸性溶液对头发没有明显影响(或溶液碱性越强对头发的损害越大);
【分析交流】洗发时先用洗发液再用护发素;因为洗发液显碱性,洗去头发上的油污,护发素显酸性,中和洗发液的碱性,保护头发;
【知识拓展】不同人头发的主要成分是相同的,故得到的结论应该是一样的.
答案:
提高测定pH的准确性(或减小实验误差);
【实验结论】碱性溶液对头发影响大,酸性溶液对头发没有明显影响(或溶液碱性越强对头发的影响越大.)
【分析交流】先用洗发液后用护发素; 护发素与洗发液发生中和反应,使头发处于中性或弱酸性的环境中,有利于头发的健康
【知识拓展】是; 因为头发的主要成分相同.
点评 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.该题通过对日常生活中知识的探究,使同学们能将所学知识更好地应用于生活,同学们要具体分析,综合掌握.


科目:初中化学 来源: 题型:解答题
| FeCl3溶液 | FeSO4溶液 | |
| 滴入NaOH溶液的现象 | 生成红褐色沉淀 | 先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色沉淀. |
化学方程式 | FeCl3+3NaOH=Fe(OH)3↓+3NaCl 基本反应类型属于①复分解反应. | FeSO4+2NaOH=Fe(OH)2↓+Na2SO4 ②Fe(OH)2+O2+H2O=4Fe(OH)3 (完成并配平此方程) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用烧杯量取9.3 毫升硫酸铜溶液 | |
| B. | 不锈钢不是纯净物 | |
| C. | 硫酸在水中电离出氢离子和硫酸根离子,其水溶液呈电中性 | |
| D. | 加到双氧水里的二氧化锰在反应前后质量和化学性质均不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
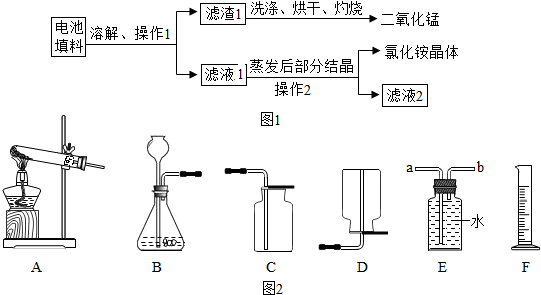
| 验实号编 | 试剂 | 前10 min内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30 mL 30% | 564.3 |
| b | 含杂质的锌 | 30 InL 30% | 634.7 |
| c | 纯锌 | 30 mL 20% | 449.3 |
| d | 纯锌 | 40 mL 30% | 602.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
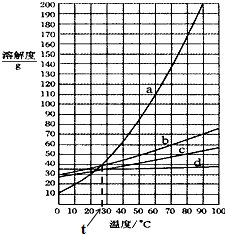 如图是a、b、c、d四种固体物质的溶解度曲线;如表是这些固体物质在部分温度时的溶解度.
如图是a、b、c、d四种固体物质的溶解度曲线;如表是这些固体物质在部分温度时的溶解度. | NaCl | KCl | NH4Cl | KNO3 | |
| 10°C | 35.8g | 31.0g | 33.3g | 20.9g |
| 60°C | 37.3g | 45.5g | 55.2g | 110.0g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 溶液 | A | B | C | D |
| X | 盐酸 | 氢氧化钠 | 盐酸 | 氢氧化钠 |
| Y | 水 | 水 | 氢氧化钠 | 盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2010年5 月12 日,在苍茫海水中沉没了 800 多年的“南海一号”重见天日,其中的宋代铜钱已经锈迹斑斑.已知:铜绿的主要成分是碱式碳酸铜[Cu 2( OH )2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$ 2CuO+H2O+CO2↑.某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.实验用到的主要装置如下:
2010年5 月12 日,在苍茫海水中沉没了 800 多年的“南海一号”重见天日,其中的宋代铜钱已经锈迹斑斑.已知:铜绿的主要成分是碱式碳酸铜[Cu 2( OH )2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$ 2CuO+H2O+CO2↑.某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.实验用到的主要装置如下:| 装置 质量 时间 | 装置① | 装置③ |
| 实验前 | 220.0克 | 195.0克 |
| 实验后 | 222.1克 | 199.4克 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com