
| 80 |
| x |
| 98 |
| 10g×98% |
| 142 |
| y |
| 14.2g |
| 100g+100g |


科目:初中化学 来源: 题型:
| A、属于化合物 |
| B、由碳、氢、氧三种元素组成 |
| C、每个尼古丁分子中含有3种元素 |
| D、尼古丁分子中含有氮分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 1 |
| 3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
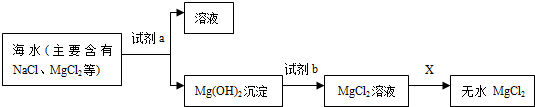
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
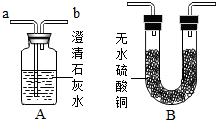 某学校化学课外活动小组,对铜制品生锈很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为Cu2(OH)2CO3,他们在探究中发现,铜绿受热分解后,除生成二氧化碳和水蒸气外,试管中还有一些黑色粉末状固体,为了更清楚地了解这种黑色粉末,同学们准备通过实验探究,进一步分析黑色固体的组成,并验证产生的气体:
某学校化学课外活动小组,对铜制品生锈很感兴趣.经查阅资料,知道铜锈的主要成份是碱式碳酸铜,俗称铜绿,化学式为Cu2(OH)2CO3,他们在探究中发现,铜绿受热分解后,除生成二氧化碳和水蒸气外,试管中还有一些黑色粉末状固体,为了更清楚地了解这种黑色粉末,同学们准备通过实验探究,进一步分析黑色固体的组成,并验证产生的气体:查看答案和解析>>
科目:初中化学 来源: 题型:
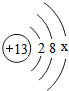 .请回答:
.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com