
 ����þ��Һ���Ժ�����������Һ��Ӧ
����þ��Һ���Ժ�����������Һ��Ӧ SO42-
SO42-  Mg2+
Mg2+  Na+
Na+���� ��1����������þ���������Ʒ�Ӧ����������þ�����������Ʒ�����Ӧ������
��2�������������ƺ�����þ��Ӧ����������þ�����������Ʒ������ķ��ţ�
��3�����ݰ�ˮ��NH3•H2O������ˮ��Һ���ܽ�������������ӷ����ش�
��4�����ݷ�Ӧ�Ļ�ѧ�����ҳ���ϵʽ��Ȼ����㼴�ɣ�
��� �⣺��1������þ���������Ʒ�Ӧ����������þ�����������ƣ�����ʵ������Ϊ������ɫ������
��2������þ���������Ʒ�Ӧ����������þ�����������ƣ���Ӧ����Һ�к��������Ӻ���������ӣ���� ��ʾNa+��
��ʾNa+�� ��ʾSO42-����Ӧ��
��ʾSO42-����Ӧ�� ��ʧ������Ϊ�����������ӽ��������������þ���������
��ʧ������Ϊ�����������ӽ��������������þ��������� ��ʾMg2+��
��ʾMg2+��
��3����ˮ��NH3•H2O����һ�ּ��ˮ��Һ���ܽ�������������ӣ�Ҳ�ܺ�����þ��Ӧ������ˮ��NH3H2O��������������Һ�о�����һ����ͬ���ӣ��������ǣ�OH-��
��4����μӷ�Ӧ��þ������Ϊx
�������֪�����ķ�Ӧ�ǣ�
Mg+H2SO4�TMgSO4+H2��
MgSO4+2NaOH=Na2SO4+Mg��OH��2����
��Mg��Mg��OH��2��
24 58
x 5.8g
$\frac{24}{58}=\frac{x}{5.8g}$ ��ã�x=2.4g
�ʴ�Ϊ����1��������ɫ��������2��SO42-��Mg2+��Na+����3��OH-����4��Mg+H2SO4�TMgSO4+H2����2.4��
���� ������Ҫ�������ʵ����ʣ����ʱҪ���ݸ������ʵ����ʣ���ϸ������������з������жϣ��Ӷ��ó���ȷ�Ľ��ۣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ���������ƴ�����ʯ�ҿ��Լ����̣����ͳɱ� | |
| B�� | �Լ�a���������ᣬҲ�������Ȼ��� | |
| C�� | ���������������仯���������������л�ѧ�仯���� | |
| D�� | ���������з����˻��Ϸ�Ӧ���ֽⷴӦ�����ֽⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
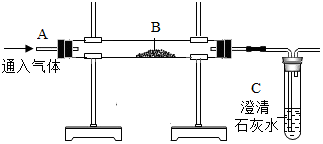 ����ͼװ���������ʵ�飺
����ͼװ���������ʵ�飺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
| �ڢ��� | �ڢ��� | �ڢ��� | |
| ϡ��������/�� | 20 | 40 | 60 |
| ������������/�� | 2.2 | m | 5.5 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com