
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:填空题
 蚊香是夏日驱除蚊虫的常用物品.丙烯菊酯(化学式C19H26O3)是蚊香中常含有的高效低毒杀虫剂.
蚊香是夏日驱除蚊虫的常用物品.丙烯菊酯(化学式C19H26O3)是蚊香中常含有的高效低毒杀虫剂.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
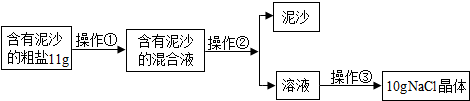
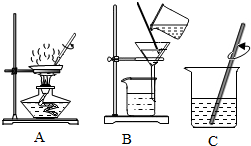
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
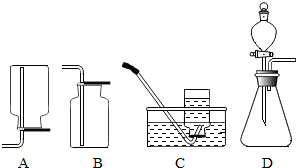 实验室制取气体的实验装置如图,请回答问题:
实验室制取气体的实验装置如图,请回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②④⑤⑥ | C. | ②③④⑤ | D. | ①②③⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
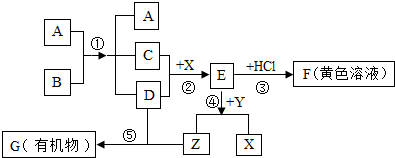
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
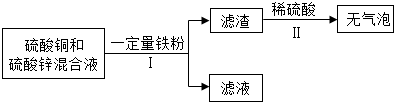
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com