
 如图是小柯同学在复习科学时,构建酸通性的“手掌图”.
如图是小柯同学在复习科学时,构建酸通性的“手掌图”.科目:初中化学 来源: 题型:选择题
| A. | 相对原子质量就是原子的实际质量 | B. | 原子的质量主要集中在原子核上 | ||
| C. | 原子是由原子核和核外电子构成 | D. | 原子的质子数等于核外电子数 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
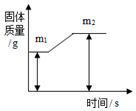 质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题.
质量守恒定律是一条重要规律,请利用该规律的相关知识回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 次氯酸钠中氯元素的化合价为-1 | |
| B. | 氯化钠中氯离子与次氯酸钠中的氯原子互为同位素 | |
| C. | 反应前氯气的质量和反应后溶液中氯元素的质量相等 | |
| D. | 氯化钠由钠元素和氯元素组成,所以为混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu$\stackrel{+HCl}{→}$CuCl2$\stackrel{+KOH}{→}$Cu(OH)2 | |
| B. | Cu$\stackrel{+O_{2}}{→}$CuO$\stackrel{+H_{2}SO_{4}}{→}$CuSO4$\stackrel{+NaOH}{→}$Cu(OH)2 | |
| C. | Cu$\stackrel{+O_{2}}{→}$CuO$\stackrel{+H_{2}SO_{4}}{→}$CuSO4$\stackrel{+Ba(OH)_{2}}{→}$Cu(OH)2 | |
| D. | Cu$\stackrel{+H_{2}SO_{4}(浓)}{→}$CuSO4$\stackrel{+NaOH}{→}$Cu(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com