
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 | |
 步骤2:取适量滤液于试管中,滴加稀硫酸。 步骤2:取适量滤液于试管中,滴加稀硫酸。 | 有 ① 生成,说明有Ba2+ |
| 步骤3:取适量步骤1中的沉淀于是试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中。 | 试管中有 ②生成,烧杯中 ③ ,结合步骤2说明沉淀是BaCO3。 |
| 步骤4:取适量滤液于试管中, ④ 。 | 试管中有蓝色沉淀生成,说明有大量的OH—,综合上面步骤可知试剂由大量Ba(OH)2和少量BaCO3组成,假设成立。 |
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验目的 | 实验方法 | 实验现象 |
| 验证鱼鳔内含O2 | ① | |
| 验证鱼鳔内含CO2 | ② | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
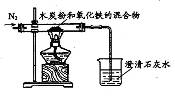
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验步骤 | 现象与结论 |
| | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
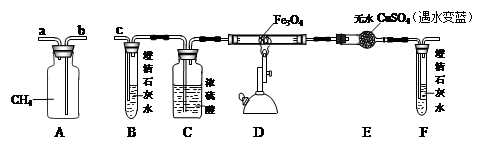
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 探究过程 | K2CO3 | (NH4)2SO4 | 结论及化学方程式 |
| ①、分别取碳酸钾和硫酸铵固体,加足量水搅拌,测其温度变化情况 | 得到澄清溶液; 温度无明显变化 | 得到澄清溶液; 温度明显降低 | 都易溶于水; 硫酸铵溶于水时吸收的热量大于放出的热量。 |
| ②、取①中溶液分别滴入紫色石蕊试液,观察溶液颜色变化,并判断其酸碱性 | | 变红 | 碳酸钾溶液显 性 硫酸铵溶液显 性 |
| ③、另取①中溶液分别加入足量稀盐酸,观察现象 | | 无明显现象 | 写出相关反应的化学方程式: |
| ④、再取①中溶液分别加入Ba(OH)2溶液,观察现象 | 产生 白色沉淀 | | (NH4)2SO4与Ba(OH)2溶液反应的化学方程式: (NH4)2SO4+Ba(OH)2=BaSO4↓ +2H2O+2NH3↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com