
 自行车的主要材料钢铁易生锈,请为图中标示的自行车部件各设计一种不同的、合理的防锈方法.
自行车的主要材料钢铁易生锈,请为图中标示的自行车部件各设计一种不同的、合理的防锈方法.分析 钢铁生锈的条件是钢铁与氧气和水同时接触.防止金属生锈的方法有:在金属表面涂一层油漆;在金属表面镀一层金属等.
解答 解:(1)因为自行车的车架部分是金属制成(主要是钢铁),铁同时和氧气、水接触,容易生锈.如果给车架刷漆,可以阻止铁和氧气、水接触,可以有效的防止其生锈.故答案为:刷漆;
(2)辐条也是铁制成的,起支撑作用,镀一层耐腐蚀的金属,既可以防锈,又有光泽,比较美观;故填:电镀;
(3)链条通常也是铁制成的,但它需要和齿轮摩擦,齿轮也是铁质的,时间长了,容易磨损,如果给链条涂油,可以阻止铁和氧气、水接触,有效的防止其生锈,还可起到润滑作用,减小摩擦,这样既可省力,又减少磨损,延长链条的使用寿命.故答案为:涂油.
点评 本题主要考查学生对防止铁生锈的方法的掌握,还要求学生能灵活运用各种防锈方法,把所学知识用到实际生活中,学以致用.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | ①③②⑤④⑥ | B. | ②③①④⑤⑥ | C. | ⑤③②①④⑥ | D. | ③①②④⑥⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NB | B. | BN | C. | bN | D. | B3N3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 电解水:2H2O $\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2↑ | |
| B. | 焦炭与水蒸气反应:C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO | |
| C. | 太阳光分解水:2H2O$\frac{\underline{\;\;\;TiO_{2}\;\;\;}}{太阳光}$2H2↑+O2↑ | |
| D. | 天然气与水蒸气反应:CH4+H2O $\frac{\underline{\;高温\;}}{\;}$ CO+3H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验室中氯化钡废液可直接排入下水道 | |
| B. | 利用2Cu+O2+2H2SO4(稀)═2CuSO4+2H2O的反应由铜制取胆矾 | |
| C. | 在煤矿附近建发电厂有利于减少二氧化硫排放 | |
| D. | 用废旧塑料制食品包装袋以减少“白色污染” |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
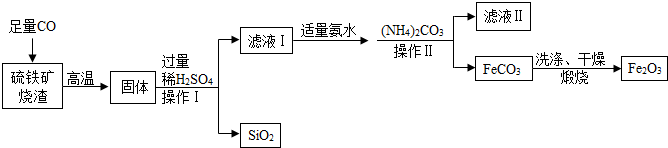
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 物 质 | Cu(OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 1.2 |
| 完全沉淀pH | 6.7 | 3.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com