
| A、10g | B、9g | C、8.5g | D、条件不足,无法确定 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| 编号 | 1 | 2 | 3 | 4 |
| 加水的质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 7.25 | 4.05 | m | 3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
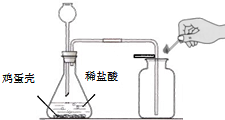 (2010?松江区一模)小张同学为了测定鸡蛋壳中碳酸钙的质量分数,进行了如下实验探究.
(2010?松江区一模)小张同学为了测定鸡蛋壳中碳酸钙的质量分数,进行了如下实验探究.| 至质量不减少 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源:北京期末题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com