
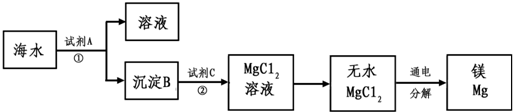
从海水中提取镁,常采用把贝壳灼烧后加入海水贮水池中,使海水中的Mg2+生成Mg(OH)2白色沉淀。灼烧贝壳的方程式为__________________,产生Mg(OH)2沉淀的反应方程式为_________,生石灰与水反应生成_________,反应方程式为__________________,该反应能够_________,可以煮熟鸡蛋;生石灰常用作黏合剂,可以把细纱、黏土等牢牢黏合在一起,自身变成__________________,化学方程式为_________________。
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
我国京沪高铁上的高速动车组最高运行时速达到486.1千米,为世界铁路运营试验最高速。京沪高铁上每段钢轨长500米,重30吨;动车组采用了铝合金车体,车窗全部采用双层、贴膜玻璃;并通过铜合金导线为动车组提供电力。
(1)生产钢轨要用到大量的钢铁。写出以磁铁矿(主要成分Fe3O4)为原料炼铁的化学方程式:_______,该反应_______(填“是”或“不是”)置换反应。
(2)用作京沪高铁动车组导线的铜合金的硬度比纯铜_______(填“大”或“小”)。
(3)铝合金车体的重量比碳钢车体重量轻40%,其节能环保优越性能更为突出。已知防锈铝(铝镁合金)是铝合金的一种,若将防锈铝粉末放入足量的硫酸铜溶液中反应后过滤,所得固体中含有的金属单质是_______(填序号)。
①Al ②Mg ③Cu ④Al和Cu、
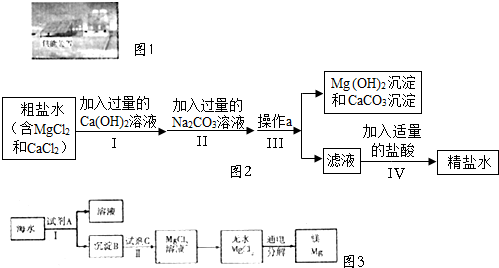
(4)镁也是21世纪重要的轻型环保材料。占地球表面积70%的海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
海水中的MgCl2  Mg(OH)2
Mg(OH)2 MgCl2·6H2O
MgCl2·6H2O MgCl2
MgCl2 Mg
Mg
试写出工业上采用在通电的条件下分解熔融氯化镁的方法得到金属镁的化学方程式:
______________。该过程中,电能转化为_______能。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com