
分析 由CaCO3+2HCl═CaCl2+H2O+CO2↑,CO2+Ca(OH)2═CaCO3↓+H2O可知,CaCO3~CO2~CaCO3,将气体通过足量的澄清石灰水得到5g白色沉淀,说明反应生成的碳酸钙的质量是5g,进一步说明锌和碳酸钙的混合固体中碳酸钙的质量是5g;
根据碳酸钙的质量可以计算与稀盐酸反应生成二氧化碳的质量,进一步可以计算2.4g混合气体中氢气的质量,从而可以计算混合固体中锌的质量分数.
解答 解:(1)因为二氧化碳和澄清石灰水反应生成碳酸钙的质量和锌和碳酸钙的混合固体中碳酸钙的质量相等,因此混合固体中碳酸钙的质量是5g.
故填:5.
(2)设反应生成二氧化碳的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
5g x
$\frac{100}{5g}$=$\frac{44}{x}$,
x=2.2g,
则氢气的质量为:2.4g-2.2g=0.2g,
故填:0.2.
(3)设锌的质量为y,
Zn+2HCl═ZnCl2+H2↑,
65 2
y 0.2g
$\frac{65}{y}$=$\frac{2}{0.2g}$,
x=6.5g,
混合固体中锌的质量分数为:$\frac{6.5g}{6.5g+5g}$×100%=56.5%,
答:混合固体中锌的质量分数为56.5%.
点评 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙和水,要能够根据反应的关系找出碳酸钙的转化关系,这是解答的关键,要注意理解.


科目:初中化学 来源: 题型:解答题
 A、B两种固体物质的溶解度曲线如图所示,请回答问题:
A、B两种固体物质的溶解度曲线如图所示,请回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 红磷在氧气中燃烧时,产生大量白色烟雾 | |
| B. | 木炭在氧气中燃烧时,发出白光,生成黑色固体 | |
| C. | 铁丝在氧气中剧烈燃烧时,火星四射,生成黑色固体 | |
| D. | 硫粉在氧气中燃烧时,发出蓝紫色火焰,闻到刺激性气味 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20% | B. | 30% | C. | 25% | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
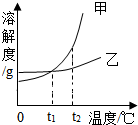 甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是( )| A. | t1℃时,甲和乙的饱和溶液各50g,含溶质的质量一定相等 | |
| B. | 将甲、乙的饱和溶液从t2℃降到t1℃时,析出甲的质量大 | |
| C. | 将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法 | |
| D. | 依据溶解度曲线可判断,甲的溶解度比乙的大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 事实 | 解释 | |
| A | 活性炭净水 | 活性炭疏松多孔,有很强的吸附能力 |
| B | 在密闭容器中,蜡烛燃烧一段时间后熄灭 | 说明物质燃烧需要氧气 |
| C | 将铝丝浸入硫酸铜的溶液中,铝丝表面无明显现象 | 铜比铝活泼 |
| D | 25m3的氧气可以转入0.024m3的钢瓶中 | 氧气分子间的间隔变小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com