
【题目】下列是初中化学常见仪器与实验。
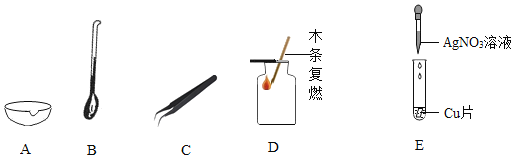
(1)A图中仪器的名称是_______。
(2)取用块状大理石用到的是_______(填字母)图中仪器。
(3)D图为检验氧气是否收集满的操作,请将明显的错误加以改正_______。
(4)E图中能够说明Cu和Ag活动性顺序的现象是_______。
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:初中化学 来源: 题型:
【题目】下表是元素周期表的部分信息,请根据下表回答有关问题:
3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(1)铝元素的相对原子质量为____________;
(2)表中与锂元素化学性质相似的元素是__________;
(3)由第7号元素和第12号元素的原子形成化合物的化学式为__________;
(4)某离子带1个单位正电荷,其结构示意图如图所示:![]() ,该离子的符号是____________,该元素位于第_____周期;
,该离子的符号是____________,该元素位于第_____周期;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究物质的溶解对于生产、生活有着重要意义。
①下表是硝酸钾的部分溶解度数据。
温度(℃) | 20 | 40 | 60 | 80 |
溶解度(g/100g水) | 31.6 | 63.9 | 110 | 169 |
由表中数据可知,硝酸钾的溶解度随温度升高而______ (选填“变大”或“变小”)。60℃时硝酸钾饱和溶液中,溶质与溶剂的质量比为_______,能将该饱和溶液转化为不饱和溶液的一种方法是________ 。
②探究20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。向硝酸钾中分批加水,充分搅拌,现象如下图所示:
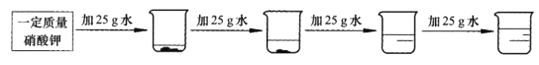
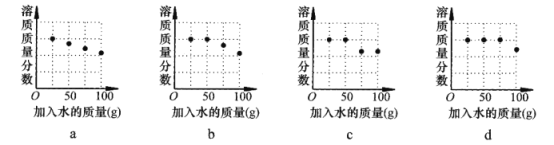
坐标图中,符合实验结果的描点可能是___________(选填编号)。
③取等质量甲和乙两种物质(均不含结晶水)进行如下图所示实验,最终烧杯中析出固体的质量乙大于甲。
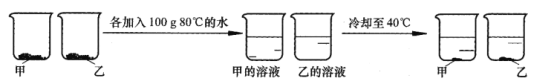
40℃时,甲的溶解度 ______(选填“大于”“等于”或“小于”)乙的溶解度根据本实验结果,能否判断40~80℃间甲、乙哪种物质的溶解度变化随温度影响更大_____ (选填“能”或“不能”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语(元素符号、离子符号、化学式、化学方程式)填空:
(1)三个亚铁离子_____;
(2)碳的+2 价氧化物_____;
(3)由空气中含量最多的元素、地壳中含量最多的非金属元素和地壳中含量最多的金属 元素共同组成的化合物的化学式_____;
(4)在尘埃的催化作用下,二氧化硫和氧气反应生成三氧化硫(SO3):_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】推理是化学学习中常用的思维方法,下列推理正确的是( )
A. 碱性溶液能使酚酞溶液变红色,能使酚酞溶液变红色的溶液一定显碱性
B. 离子是带电的微粒,带电的微粒一定是离子
C. 氧化物中一定含有氧元素,含氧元素的化合物一定是氧化物
D. 置换反应的生成物是一种单质和一种化合物,生成一种单质和一种化合物的反应一定是置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“鱼浮灵”是常用的化学增氧剂,主要成分是过氧碳酸钠(2Na2CO33H2O2),溶于水能迅速增加水体溶氧量,提高鱼苗及活鱼运输成活率。某化学兴趣小组对“鱼浮灵”的化学性质、增氧原理进行了探究。
(查阅资料)a.过氧碳酸钠具有碳酸钠和过氧化氢的双重性质,其水溶液中含有Na+、OH-、CO32-、H2O2。
b.Na+不能催化过氧化氢分解。
c.相同温度下,pH相同的溶液,OH-的浓度也相同。
探究一过氧碳酸钠的化学性质
实验步骤 | 实验现象 | 实验解释(化学方程式) |
1.取样,溶于水,滴加_______溶液 | 有白色沉淀生成 | / |
2.取样,溶于水,加入二氧化锰粉末 | _______ | _______ |
探究二“鱼浮灵”增氧原理
(提出问题)过氧碳酸钠溶液中的哪种微粒对过氧化氢分解有催化作用?
(猜想假设)猜想一:CO32- 猜想二:OH-猜想三:______________
(实验过程)相同温度下,进行H2O2溶液以及H2O2溶液中分别加Na2CO3、NaOH的实验,测定相同时间内溶液的pH、溶解氧含量(mg/L),数据如下:
实验序号 | 1 | 2 | 3 | 4 |
试剂 | H2O2 | H2O2+Na2CO3 | H2O2+NaOH | H2O2+NaOH |
pH | 6.01 | 8.14 | 8.14 | 9.26 |
溶解氧 | 6.44 | 9.11 | 9.11 | 10.97 |
(实验结论)对比实验数据,证明猜想_______正确。
(反思交流)设计实验2、3的目的是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验课上,老师知道某兴趣小组进行粗盐提纯的实验,邀请你帮助他们完成下面的实验报告。
(实验名称)粗盐的提纯
(查阅资料)
(1)粗盐中含有泥沙及少量可溶性MgCl2、CaCl2、Na2SO4等杂质。
(2)Ba(OH)2是一种易溶于水的强碱。
(主要玻璃仪器)量筒、烧杯、漏斗、玻璃棒、胶头滴管、酒精灯
(主要试剂)粗盐样品、稀盐酸、BaCl2溶液,NaOH溶液,Na2CO3溶液,蒸馏水
(实验过程)
步骤及目的 | 过程及说明 |
一、去除粗盐 中的泥沙 | 1.称取粗盐样品10.0g,用蒸馏水充分溶解 2.过滤去除泥沙的溶液I 以上两步操作中均需要使用到玻璃棒,玻璃棒的作用分别是:溶解时:____; 过滤时:____。 |
二、去除可溶 性杂质 | 将溶液I按如图流程图进行处理:
1、加入“过量NaOH溶液时”,发生反应的化学方程式是____。 2、过滤后,所得的滤渣成分有____种。 3、判断“稀盐酸适量”的方法是____。 |
三、获得产品 | 将溶液Ⅱ注入____(填仪器名称)中,蒸发结晶,观察到____,停止加热,利用余热蒸干。装置完全冷却后,获得干燥的产品9.4g。 |
四、数据处理 | 该粗盐样品中氯化钠的质量分数是94% |
(结果与反思)
(1)实验操作、试剂和装置均不存在问题,老师却指出该样品中氯化钠的质量分数不是94%,原因是____。
(2)小明提出,如果步骤二中只调换“过量的NaOH溶液”与“过量的BaCl2溶液”的加入顺序,对除杂结果也不会产生影响,你____(填“同意”或“不同意”)小明的观点。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E、F、G、Y为初中化学常见物质,其中C、E、G属于单质,Y是一种有毒气体,反应①是炼铁工业中的主要反应,它们之间的相互转化关系如图所示:

(1)D物质的化学式是_____,E物质的化学式是_____;
(2)反应①的化学方程式为_____,此反应中被氧化的物质是_____(写化学式)
(3)X是_____和_____(均写化学式)的混合溶液,当_____的情况下将没有E生成。
(4)反应②中生成红色固体的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列应用及相应原理(用化学方程式表示)都正确的是( )
A. 用稀盐酸除铁锈Fe2O3+6HCl=2FeCl2+3H2OB. 用二氧化碳制碳酸饮料CO2+H2O=H2CO3
C. 用电解水的方法测定水的组成2H2O=2H2↑+O2↑D. 用氢氧化钠制碳酸钠CaCO3+NaOH=Ca(OH)2 + Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com