
【题目】一定质量的CH4可与常见物质M反应,同时放出少量热量;将所得产物Cu2O与O2反应又生成M,同时放出较多热量。其反应原理如下图所示。下列说法正确的是

A.M中铜元素的质量分数比Cu2O中的高
B.理论上反应每生成44gCO2,同时生成18gH2O
C.理论上每16gCH4参与反应,最终消耗64gO2
D.过程①可将CH4中的部分能量储存于Cu2O中
【答案】C
【解析】
如图所示,CH4与常见物质M反应生成Cu2O、二氧化碳和水,Cu2O与O2反应生成M,则M为CuO,则有:
A、CuO中铜元素的质量分数为![]() ,Cu2O中铜元素的质量分数为
,Cu2O中铜元素的质量分数为![]() ,Cu2O中铜元素的质量分数比CuO中的高,A选项说法不正确,不符合题意;
,Cu2O中铜元素的质量分数比CuO中的高,A选项说法不正确,不符合题意;
B、根据反应过程、由元素守恒可知生成物二氧化碳中的碳元素来自于甲烷,水中的氢元素来自于甲烷,44gCO2中碳元素的质量为![]() ,则参加反应的甲烷的质量为
,则参加反应的甲烷的质量为![]() ,设16g甲烷反应生成水的质量为
,设16g甲烷反应生成水的质量为![]() ,由氢元素守恒则有
,由氢元素守恒则有![]() ,解得
,解得![]() ,因此理论上反应每生成44gCO2,同时生成36gH2O,B选项说法不正确,不符合题意;
,因此理论上反应每生成44gCO2,同时生成36gH2O,B选项说法不正确,不符合题意;
C、由反应过程可知,CH4与常见物质CuO反应生成Cu2O、二氧化碳和水,反应的方程式为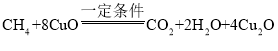 ,由方程式可知每16份质量的甲烷与640份质量的氧化铜恰好反应,Cu2O与O2反应生成CuO,反应的方程式为
,由方程式可知每16份质量的甲烷与640份质量的氧化铜恰好反应,Cu2O与O2反应生成CuO,反应的方程式为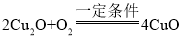 ,由方程式可知每32份质量的氧气参与反应生成320份质量的氧化铜,由两个反应之间的关系可知理论上每16份质量的CH4参与反应,最终消耗64份质量的O2,即理论上每16gCH4参与反应,最终消耗64gO2,C选项说法正确,符合题意;
,由方程式可知每32份质量的氧气参与反应生成320份质量的氧化铜,由两个反应之间的关系可知理论上每16份质量的CH4参与反应,最终消耗64份质量的O2,即理论上每16gCH4参与反应,最终消耗64gO2,C选项说法正确,符合题意;
D、过程①CH4与常见物质M反应生成Cu2O、二氧化碳和水,该过程释放能量,可将反应物CH4和M中的部分能量储存于Cu2O、二氧化碳和水中,D选项说法不正确,不符合题意。故选C。


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:初中化学 来源: 题型:
【题目】在2020年春节伊始,我国爆发了新型冠状病毒肺炎,给人民的生命带来严重的威胁,给国家人民的财产带来严重的损失,全国人民众志成城抗击新型冠状病毒肺炎。在众多的措施中有一条就是要勤消毒。84消毒液有效成分为次氯酸钠和二氧化氯(ClO2),是常用消毒剂。
(1)将氯气通入氢氧化钠溶液中可以得到次氯酸钠,根据反应原理推断次氯酸钠的化学式。其反应原理:Cl2 + 2NaOH= NaCl +H2O + ______,次氯酸钠中氯元素的化合价____;
(2)次氯酸钠属于_____________(填序号)。
A 酸 B 碱 C 氧化物 D 盐
(3)次氯酸钠固体在光照的情况下分解为一种常见的化学物质和空气中体积分数为21%的气体,写出其化学反应方程式:___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是碳酸钠和氯化钠的溶解度曲线,下列叙述错误的是( )

A.![]() ℃时,
℃时,![]() 的溶解度大于
的溶解度大于![]() 的溶解度
的溶解度
B.![]() ℃时,
℃时,![]() 和
和![]() 溶液中所含溶质质量一定相等
溶液中所含溶质质量一定相等
C.![]() ℃时,将
℃时,将![]() 的饱和溶液加热蒸发,一定有晶体析出
的饱和溶液加热蒸发,一定有晶体析出
D.![]() 固体中含有少量的
固体中含有少量的![]() ,可用降温结晶的方法提纯
,可用降温结晶的方法提纯![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向5.6g含两种杂质的铁粉样品中加入足量的稀盐酸,充分反应后共产生0.2g氢气,则该样品中所含杂质可能是
A.锌和铜B.锌和镁
C.铝和镁D.碳和铜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中Na2CO3的质量分数。他们取了6g纯碱样品放入烧杯中,再将80g一定溶质质量分数的稀盐酸分4次加入该烧杯中,充分反应后测得实验数据如下表(不考虑CO2溶解于水)
实验次数 | 1 | 2 | 3 | 4 |
加人稀盐酸的质量/g | 20 | 20 | 20 | 20 |
烧杯中剩余物质的质量/g | 25.2 | m | 63.8 | 83.8 |
(1)表格中m的值为_____。
(2)样品中Na2CO3的质量分数是多少? (写出计算过程,计算结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以FeSO4·7H2O为原料制备铁红(Fe2O3)的一种方法如下:

已知“沉淀”时的主要反应为:![]()
(1)FeO(OH)中铁元素的化合价为_______。FeO(OH)可表示为mFe2O3·nFe(OH)3,![]() =_____________。
=_____________。
(2)“沉淀”时需控制溶液的pH与反应的温度。
①“沉淀”时调节溶液的初始pH约为4,过程中应始终保持溶液的pH为3.0~4.5,需不断加入物质Z调节溶液的pH,Z应具备的性质有__________(填字母)。
A 能与酸反应
B 能与碱反应
C 不与FeO(OH)反应
②“沉淀”时反应温度不宜过高,其原因是_______。
(3)“过滤”后需对固体进行洗涤与干燥。洗涤时被除去的沾于固体表面的阴离子为__________(填离子符号)。
(4)“煅烧”时反应的化学方程式为________。
(5)如图为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。煅烧温度较低时,产品中Fe2O3质量分数较低,其原因是___________。当煅烧温度达800℃时,继续升高温度,产品中Fe2O3质量分数降低,且铁元素质量分数升高,所得产品发黑,其可能原因是_______。
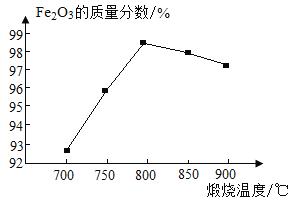
(6)用该方法制备Fe2O3,计算理论上13.9 t FeSO4·7H2O(相对分子质量为278)可制得Fe2O3的质量(写出计算过程)。_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】新冠肺炎疫情防控期间,湘潭市各学校开展全域喷洒低浓度“84”消毒液进行消毒。“84”消毒液的有效成分是NaClO(次氯酸钠),模拟制备“84”消毒液的流程如下图所示,其中A是密度最小的气体,B俗称烧碱,Cl2是一种黄绿色的有毒气体。请回答下列问题:
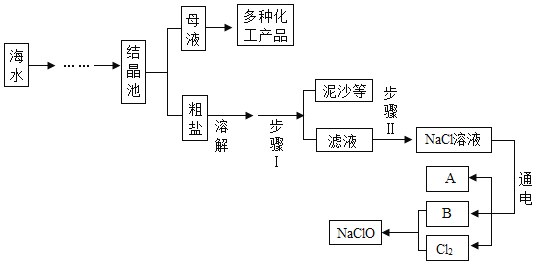
(1)A的化学式为_____,B的化学式为_______。
(2)溶解过程中玻璃棒的作用是____,步骤I中主要的操作名称是______。
(3)步骤Ⅱ中,通常用碳酸钠来除去滤液中的氯化钙杂质,请写出有关反应的化学方程式____,该反应属于___反应(填基本反应类型)。
(4)电解水时,一般在水中加入少量硫酸钠或氢氧化钠的目的是_______,不能加入NaCl的原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com