
中和反应是放热反应。取10 ml溶质质量分数为10%的NaOH溶液(密度1.10g/ml)置于烧杯中(并滴入2滴酚酞),向烧杯中逐滴加入稀盐酸。随着盐酸的滴入,烧杯中溶液颜色从红色逐渐变浅,当加入10 ml稀盐酸时,溶液恰好变为无色。烧杯中溶液温度与加入盐酸体积之间关系如图所示。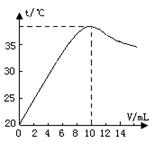
(1)当加入4ml稀盐酸时,烧杯中溶液的溶质为
(写化学式)
(2)试解释烧杯中溶液温度随加入盐酸的体积发生变化的
原因 。
(3)当盐酸与氢氧化钠恰好中和时生成氯化钠多少克?
(精确到0.1g)
(1)NaOH NaCl
(2)中和反应放热,随着反应的进行,放出热量增加,溶液温度逐渐升高,加入10毫升稀盐酸时恰好完全反应,溶液温度最高。继续加入盐酸后,溶液被稀释冷却,温度逐渐下降。
(3)1.6g
解析试题分析:
(1)由图可知,当加入10毫升稀盐酸时恰好完全反应,故加入4ml稀盐酸时,氢氧化钠过量,此时烧杯中溶液的溶质为NaOH和NaCl;
(3)根据质量守恒定律利用氢氧化钠与氯化钠的质量比即可求出氯化钠的质量。
解:设生成氯化钠的质量为x
NaOH + HCl = NaCl + H2O
40 58.5
1.1mL×1.1g/mL×10% x
40/( 1.1mL×1.1g/mL×10%)=58.5/x
x=1.6g
答:略
考点:中和反应、利用化学方程式的计算


科目:初中化学 来源: 题型:计算题
某兴趣小组的同学为了测定碳酸钠样品(只含有氯化钠,不含其它杂质)中碳酸钠的含量,取该混合物样品与适量稀盐酸恰好完全反应,有关实验数据见附表.
附表:实验数据
| | 反应前 | 反应后 | |||
| 实验数据 | 烧杯的质量/g | 稀盐酸的质量/g | 混合物样品的质量/g | 烧杯和其中混合物的质量/g | |
| 40.6 | 123.4 | 12 | 171.6 | | |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(7分)学过金属活动性后,秦思同学通过实验探究锌粉与硝酸亚铁和硝酸银两种盐溶液的反应。实验现象和数据如下: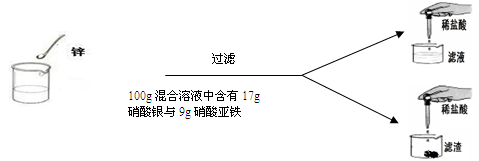
| | 第一次 | 第二次 | 第三次 | 第四次 |
| 硝酸亚铁与硝酸银的混合溶液 | 100g | 100g | 100g | 100g |
| 锌粉 | 2g | 3.25g | m | 9.75g |
| 向滤液中加入稀盐酸后的实验现象 | 产生白色沉淀 | 无明显现象 | 无明显现象 | 无明显现象 |
| 向滤渣中加入100 g稀盐酸后的实验现象 | 无明显现象 | 无明显现象 | 产生气泡,溶液变为浅绿色 | 现象与第三次相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(3分)某化学兴趣小组的同学对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。他们称取了13.6g固体样品,用图1所示的装置继续实验,测定的部分数据如图2所示。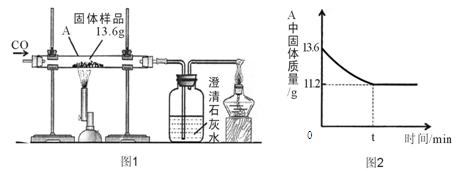
请计算:固体样品中氧化铁的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(7分))课外活动时,同学们采用以下两种方法测定某氯化钠溶液的溶质质量分数。
(1)【化学方法】向一定量氯化钠溶液中加入足量硝酸银溶液,得到2.87g氯化银固体,则该氯化钠溶液中氯化钠的质量为多少?(根据化学方程式列式计算)
经多次实验测定,该溶液的溶质质量分数为10%。
(2)【物理方法】取一定量该溶液进行蒸发,测量实验数据如下:
| 蒸发皿的质量(g) | 25.0 |
| 蒸发皿+食盐溶液(g) | 45.0 |
| 蒸发皿+食盐晶体(g) | 27.4 |
| 数据处理 | 溶液的溶质质量分数为 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(3分)电动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点是可以充电循环使用,电瓶内发生的化学反应是:
PbO2(固)+ 2H2SO4 + Pb = 2PbSO4↓+ 2H2O
某电瓶中装有36%的稀硫酸1200 g,电瓶工作时有310.5 g的铅参加反应。试计算:
(1)原稀硫酸中所含溶质的质量是 g。
(2)电瓶工作时消耗硫酸的质量。
(3)反应后硫酸溶液中溶质的质量分数。(最后结果精确到0.01%)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(6分)为了测定某品牌小苏打样品中碳酸氢钠的质量分数,兴趣小组进行了如下图所示的实验(假设该样品中只含有氯化钠一种杂质)。
请计算:
生成CO2气体的质量;
样品中碳酸氢钠的质量分数。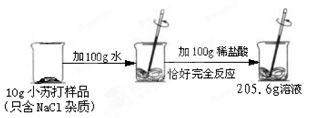
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(6分)黄铜(由铜和锌形成的合金)有较强的耐磨性能、可塑性好、易加工,在生活中有广泛的用途,可以制作机器零件、仪表等.某同学为了测定某黄铜屑样品的组成,分四组取样品与稀硫酸反应,其实验数据记录如下表: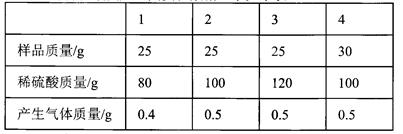
(1)通过分析上述数据可知,第 实验黄铜样品和稀硫酸恰好完全反应;
(2)黄铜合金中锌的质量为 g
(3)列式计算所用稀硫酸中硫酸的质量分数?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com