
A��B��C��D�dz��л�ѧ�еij������ʣ������������ж�����XԪ�أ���֪����XԪ���ǵؿ��к�����ߵ�Ԫ�آ�AΪ���ʣ�B��C��DΪ������
��B�Dz�������ЧӦ����Ҫ�����C�������ڽ���ҵ��C��ϡ���ᷴӦ�ɲ���B��D��һ���Σ���D�뱥��ʯ��ˮ��Ӧ������C����һ�ּ�
��ش�
��1��XԪ������ Ԫ�أ���ѡ��������ǽ�������
��2��C�Ļ�ѧʽΪ ��
��3��д��A������Ӧ�Ļ�ѧ����ʽ ��
��4��д��B�뱥��ʯ��ˮ��Ӧ�Ļ�ѧ����ʽ ��
��5��д��D��һ����; ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
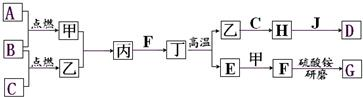
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
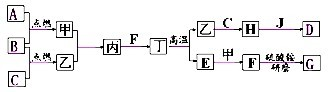
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
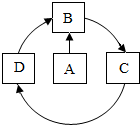 A��B��C��D�dz��л�ѧ�α��г��ֵĸ�����ͬ��4�����ʣ����Ƕ�������ͬ��һ��Ԫ�أ�����A��һ�ֺ�ɫ��ĩ������֮���ת����ϵ��ͼ��ʾ�����������Ȼ��ش�
A��B��C��D�dz��л�ѧ�α��г��ֵĸ�����ͬ��4�����ʣ����Ƕ�������ͬ��һ��Ԫ�أ�����A��һ�ֺ�ɫ��ĩ������֮���ת����ϵ��ͼ��ʾ�����������Ȼ��ش�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
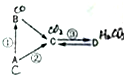 A��B��C��D�dz��л�ѧ�������������ʣ����Ƕ�����ͬһ��Ԫ�أ�ͨ�������A�ǹ��嵥�ʣ�B��C�����壬����C�ܵ�������ЧӦ������֮���ת����ϵ��ͼ��ʾ����������ʾһ��������ת������һ�����ʣ������ַ�Ӧ�������ͷ�Ӧ��������ȥ��
A��B��C��D�dz��л�ѧ�������������ʣ����Ƕ�����ͬһ��Ԫ�أ�ͨ�������A�ǹ��嵥�ʣ�B��C�����壬����C�ܵ�������ЧӦ������֮���ת����ϵ��ͼ��ʾ����������ʾһ��������ת������һ�����ʣ������ַ�Ӧ�������ͷ�Ӧ��������ȥ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com