
【题目】草酸的化学式为H2C2O4,甲、乙两同学对草酸受热分解产物的检验做了探究:
(1)猜想与假设:第一种:草酸分解产物是CO2和H2;第二种:草酸分解产物是CO2、CO和H2O;第三种:草酸分解产物是CO2和H2O。
(2)实验装置的设计(图中铁架台略去)甲同学设计了如图1所示的装置。乙同学设计了如图2所示的装置。
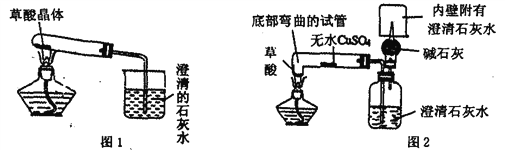
(3)实验:甲同学按图1装置实验,观察到澄清石灰水变浑浊。乙同学按图2装置实验,观察到无水硫酸铜由白色变成蓝色,澄清的石灰水变浑浊,且生成的气体通过碱石灰后,在尖嘴处点燃后能燃烧,在火焰上方罩一个内壁附有澄清石灰水的烧杯,澄清的石灰水变浑浊。
(4)结论:第___种猜想是正确的,请写出草酸受热分解的化学反应方程式__。
(5)反思与评价:
乙同学认为甲同学设计的实验装置有缺陷。由于试管口向下倾斜,而且草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中常会出现熔融的草酸流进导管而影响后续实验。甲同学认为乙同学的设计是科学合理的。请你谈谈图2装置优于图1装置之处:
第一点:__________。第二点:_______________。
第三点:_______________。
乙同学设计的图2装置也能证明产物中无H2,证明方法是______________。
【答案】 第二种 H2C2O4![]() CO2↑+CO↑+H2O 试管底部弯曲避免了草酸晶体熔化后流进导管 乙同学设计的装置可同时证明CO2、CO、H2O的存在 乙同学的设计能防止CO对空气的污染或乙同学的设计可以证明H2不存在(答到以上三点即可) 在尖嘴处点燃气体,火焰上方罩一个干冷的烧杯,烧杯内壁没有水珠生成
CO2↑+CO↑+H2O 试管底部弯曲避免了草酸晶体熔化后流进导管 乙同学设计的装置可同时证明CO2、CO、H2O的存在 乙同学的设计能防止CO对空气的污染或乙同学的设计可以证明H2不存在(答到以上三点即可) 在尖嘴处点燃气体,火焰上方罩一个干冷的烧杯,烧杯内壁没有水珠生成
【解析】本题考查了实验探究物质的组成成分,常见气体的检验与除杂方法,化学方程式的书写等。
(4)甲同学按图1装置实验,观察到澄清石灰水变浑浊,说明气体中含有二氧化碳;
乙同学按图2装置实验,观察到无水硫酸铜由白色变成蓝色,说明气体中含有水,澄清的石灰水变浑浊,说明气体中含有二氧化碳,且生成的气体通过碱石灰后,在尖嘴处点燃后能燃烧,在火焰上方罩一个内壁附有澄清石灰水的烧杯,澄清的石灰水变浑浊,说明气体中含有一氧化碳;
结论:第二种猜想是正确的,草酸受热分解的化学反应方程式为:H2C2O4 ![]() CO2↑+CO↑+H2O;
CO2↑+CO↑+H2O;
(5)图2装置优于图1装置之处:试管底部弯曲避免草酸晶体熔化后流进导管;装置可同时证明二氧化碳、一氧化碳、水的存在;乙同学的设计能防止CO对空气的污染;乙同学的设计可以证明H2不存在;氢气在空气中点燃生成水。乙同学设计的图2装置也能证明产物中无H2,证明方法是:在尖嘴处点燃气体,火焰上方罩一个干冷的烧杯,烧杯内壁没有水珠出现。


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是
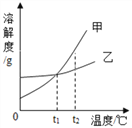
A. 甲物质的溶解度比乙物质的溶解度大
B. 甲物质溶液从t2℃降到t1℃,一定有晶体析出
C. t1℃时,甲和乙的饱和溶液中溶质的质量分数一定相等
D. 若甲物质中混有少量乙物质,可用蒸发结晶的方法提纯甲
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碘酸碘化学式为I(IO3)3,下列关于该物质的说法正确的是
A. I(IO3)3中总共有12个原子
B. I(IO3)3的相对分子质量为127×3+127×3+16×9
C. I(IO3)3和I2O4比较,I元素的质量分数前者更大
D. I(IO3)3中I元素的质量分数为![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某补钙剂说明书的部分信息如图所示,现用20片该药剂制成的固体粉末与40g稀盐酸混合(其他成分不与盐酸反应),稀盐酸平均分成4次加入烧杯中,实验数据见下表:

实验序号 | 加入稀盐酸的质量/g | 固体粉末剩余质量/g |
1 | 10 | 18.9 |
2 | 10 | 17.8 |
3 | 10 | 16.8 |
4 | 10 | m |
(1)该瓶补钙剂属于__________。(填物质分类)
(2)表格中的m=________。
(3)求稀盐酸的浓度____________。(请根据化学方程式写出完整的计算步骤)
(4)该瓶补钙剂含有碳酸钙________g。(结果保留1位小数)
(5)请根据上述内容,在下图中补全图像。
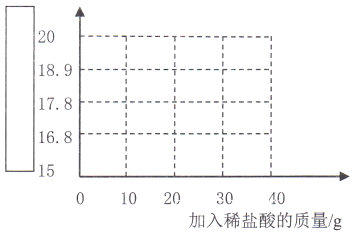 ___________
___________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是()
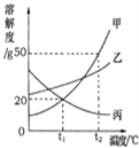
A. 将t2℃甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液溶质质量分数由大到小的选项是乙>甲>丙
B. t2℃时,将30g甲物质加入到50g水中不断搅拌,形成的溶液中溶质的质量分数是37.5%
C. 要从甲物质的饱和溶液中获得晶体甲,可采用降温结晶的方法
D. 将丙物质的饱和溶液转化为不饱和溶液可以采用加水或降温的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国劳动人民早在五千年前就会使用木炭炼铜。某化学兴趣小组在实验宝里模拟炼铜,开展如下图所示的探究活动。
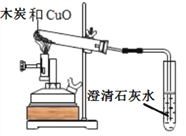
Ⅰ.验证单质碳的还原性
(1)加热固体,2min后,观察到固体变红或澄清石灰水__________,证明碳具有还原性。
(2)CuO发生________反应(填“氧化”或还原”)
(3)反应结束时,停止实验的第一步操作是__________________。
Ⅱ,探究反应后红色固体的成分
【查阅资料】(1)木炭与CuO的反应是:C+2CuO高温2Cu+CO2↑,若该反应进行的不彻底,产物中可能还含有氧化亚铜(Cu2O)。
(2)Cu2O是红色固体,能与稀硫酸反应Cu2O +H2SO4=Cu+ Cu SO4+H2O
【作出猜想】红色体的成分: a全部是Cu ;b.全部是Cu2O ;c.全部是___________
【实验步骤】取试管内红色同体,进行如下实验验证:
①取1.44g红色固体装入试管,滴入足量稀硫酸,观察到红色体部分减少,溶液变为____色,则猜想a错误。
②过滤,滤出试管中残留的红色固体,干燥,称其质为1.04g,则猜想______正确。理由是____________。
【评价反思】在的铜冶炼史中,我国劳动人民还有一项重大发明就是“湿法炼铜”,该方可用化学方程式表示为_____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校为培养学生的实验技能,设计了以下两个实验:(一)粗盐提纯;(二)实验室制取氢气和验证氢气的性质。
(一) 实验室除去粗盐中难溶性杂质的主要实验步骤有:称量与溶解、过滤、蒸发。
(1)实验中多次使用同一种玻璃仪器名称是_________。蒸发时,待蒸发皿中出现_________时停止加热,利用余热将滤液蒸干。
(2)关于蒸发叙述正确的是______(选填序号)。
a.所需仪器为酒精灯、蒸发皿、温度计
b.搅拌可以防止蒸发过程中食盐飞溅
c.加热过程中用试管夹夹住蒸发皿移动,使其均匀受热
(二)利用以下装置制备氢气,并验证氢气的性质。
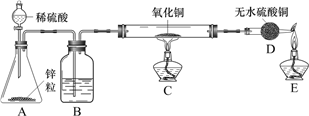
(3)实验室现有质量分数为98%的浓硫酸,需配制245 g质量分数10%的稀硫酸,配制步骤如下:
① 计算:所需质量分数98%的浓硫酸__________g;② 量取;③ 稀释。
量取浓硫酸所用的玻璃仪器有____________。简要描述浓硫酸的稀释方法_________________。
(4) 装置B的作用_____________。
(5)下列有关实验操作或现象描述不正确的是___。(填序号)
A.实验开始时,应先通入氢气,然后再点燃C处酒精灯
B.点燃C处酒精灯后,氧化铜固体由黑色逐渐变为红色
C.E处酒精灯的作用是点燃未反应的氢气
D.实验结束时,应先停止通入氢气,然后熄灭C处酒精灯
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为四种物质(KNO3、NaNO3、KCl 和NaCl)的溶解度曲线。下列说法正确的是( )
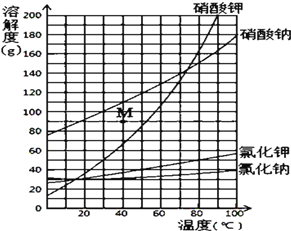
A. 四种物质中NaCl 的溶解度最小
B. 将 100℃的 KCl 溶液降温至 50℃,一定有固体析出
C. 40℃时,M 点对应的NaNO3 溶液不饱和
D. 0℃时,KNO3 溶液的质量分数为 16%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】FeSO47H2O是一种重要的食品和饲料添加剂.某工业废渣主要成分是Fe2O3,还含有CaCO8和SiO2(既不溶于水也不溶于稀硫酸),实验室用此废渣制备FeSO47H2O的流程如图1:

请根据流程图回答下列问题:
(1)稀硫酸与粉末中的氧化铁反应的化学方程式为______________________
(2)操作②的名称是_______ 。
(3)经测定,滤渣中只含有CaSO4和SiO2,你认为实验室___(填“能”或者“不能”)用粉末状的石灰石与稀硫酸反应制CO2.
(4)加入铁粉后主要现象为:铁粉逐渐溶解,____________________ 。写出Fe与Fe2(SO4)3反应的化学方程式为__________________.
(5)硫酸亚铁的溶解度曲线如图2.待结晶完毕后,过滤出晶体,用少量冰水洗涤2﹣3次.用冰水洗涤的目的是:

Ⅰ除去晶体表面附着的杂质;Ⅱ___________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com