解:(1)a是酒精灯;b是集气瓶;
(2)使用装置②时,长颈漏斗需伸入液面下,原因是:防止气体从长颈漏斗口溢出而收集不到气体;
(3)根据反应物的状态和反应条件选择发生装置:装置①适合固体加热型的气体制取,装置②适合固体和液体在常温下反应;
(4)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,写出方程式为:2KMnO
4
K
2MnO
4+MnO
2+O
2↑;实验时应在试管口放一团棉花,其作用是:防止高锰酸钾颗粒进入导气管;
(5)制取二氧化碳的药品是石灰石和稀盐酸,属于固体和液体在常温下的反应,因此应选用的发生装置是②;因为二氧化碳易溶于水,密度比空气大,故收集装置⑤(向上排空气法),故选择D;
检验CO
2气体是否已充满集气瓶的方法是:将燃着的木条放在集气瓶口,若木条熄灭,说明收集满;
(6)要测量二氧化碳的体积采用排水法,用量筒测量水的体积从而测得二氧化碳的体积;二氧化碳能溶于水,所以要在水的上方放一层植物油.植物油上方原有的空气不会溶解在水中,所以油上方的空气对实验结果没有影响.
故答案为:(1)集气瓶;酒精灯;(2)防止气体从长颈漏斗口溢出;(3)反应条件;(4)2KMnO
4
K
2MnO
4+MnO
2+O
2↑;防止高锰酸钾颗粒进入导气管;(5)D;将燃着的木条放在集气瓶口,若木条熄灭,说明收集满;(6)防止二氧化碳溶于水或与水反应;无.
分析:(1)熟练掌握常见化学仪器的名称及其用途;
(2)根据实验的注意事项回答;
(3)根据反应物的状态和反应条件选择发生装置;
(4)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,写出方程式;根据加热高锰酸钾制氧气的注意事项进行分析解答;
(5)根据反应物的状态和反应条件选择发生装置;根据气体的密度和溶解性选择收集方法;检验CO
2气体是否已充满集气瓶的方法是:将燃着的木条放置集气瓶口,看木条是否熄灭;
(6)根据二氧化碳的性质能溶于水及测定的原理分析解答.
点评:本题考查了常见气体的制取装置、收集方法等的选择及实验的注意事项,关键是明确发生装置、收集方法选择的依据.


 K2MnO4+MnO2+O2↑;实验时应在试管口放一团棉花,其作用是:防止高锰酸钾颗粒进入导气管;
K2MnO4+MnO2+O2↑;实验时应在试管口放一团棉花,其作用是:防止高锰酸钾颗粒进入导气管; K2MnO4+MnO2+O2↑;防止高锰酸钾颗粒进入导气管;(5)D;将燃着的木条放在集气瓶口,若木条熄灭,说明收集满;(6)防止二氧化碳溶于水或与水反应;无.
K2MnO4+MnO2+O2↑;防止高锰酸钾颗粒进入导气管;(5)D;将燃着的木条放在集气瓶口,若木条熄灭,说明收集满;(6)防止二氧化碳溶于水或与水反应;无.


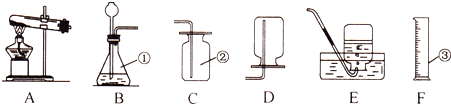

 如图所示是实验室常用的气体发生装置.
如图所示是实验室常用的气体发生装置.