

| 物质的质量 | |
| 反应前:烧杯+盐酸 | 22g |
| 10片钙片 | 8g |
| 反应后:烧杯+剩余物 | 26.7g |
分析 (1)先求出碳酸钙(CaCO3)中钙元素的质量分数,再求每片钙片中含有钙元素的质量,与标签中的含钙量比较,即可解答;
(2)根据实验的得到二氧化碳的质量和质量守恒定律,然后根据碳酸钙与盐酸反应的化学方程式即可计算出参与反应的碳酸钙的质量(即10片钙片的质量),进而计算出每片此钙片含碳酸钙的质量,再根据碳酸钙(CaCO3)中钙元素的质量分数求出钙元素的质量;
解答 解:(1)碳酸钙中钙元素的质量分数=$\frac{40}{100}$×100%=40%
每片含钙的质量=40g÷50×40%=0.32g,故含钙量是虚假;
(2)产生二氧化碳的质量为:22g+8g-26.7g=3.3g
设含碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{44}=\frac{x}{3.3g}$
x═7.5g
7.5g÷10=0.75g
答:每片此钙片含碳酸钙的质量为0.75g;
②每片此钙片的含钙量=0.75g×40%=0.3g;
答:①每片此钙片含碳酸钙的质量为0.75g.
②每片此钙片的含钙元素质量为0.3g.
点评 将质量分数的计算与生活实际相联系;计算时要理清各个量之间的关系,再结合题意进行分析解答.


科目:初中化学 来源: 题型:解答题
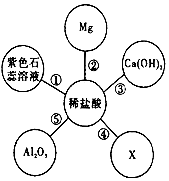 如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同,结合图示回答下列问题:
如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同,结合图示回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
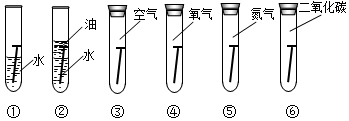
| A. | ①② | B. | ③④ | C. | ⑤⑥ | D. | ④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质名称 | 氧气 | 二氧化碳 | 氦气 | 碳酸钙 | ||
| 化学式 | Cu(OH)2 | Na | ||||
| 物质类别 | ||||||
| 式量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 净化程度最高的方法是蒸馏 | |
| B. | 在活性炭净水器里,活性炭的作用是吸附和过滤水中杂质 | |
| C. | 可用肥皂水区别硬水和软水 | |
| D. | 自来水属于混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 反应前物质的总质量/g | 反应后剩余物的总质量/g |
| 25 | 15.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
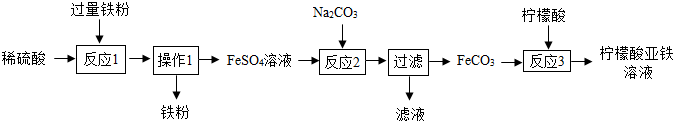
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com