
| A. | 75% | B. | 80% | C. | 85% | D. | 90% |
科目:初中化学 来源: 题型:选择题
| A. | 用霉变的花生榨取食用油 | |
| B. | 室内有燃气泄露,立即打开排气扇通风 | |
| C. | 用甲醛的水溶液浸泡海产品 | |
| D. | 久未开启的地窑、窑井,不可贸然进入 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 金属材料在生产、生活中应用广泛.
金属材料在生产、生活中应用广泛.| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
| 密度/(g•cm-3) | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
| 熔点/℃ | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 2.5~3 | 2~2.9 | 2.5 | 4~5 | 1.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 干冰升华吸热,用于制造舞台云雾 | |
| B. | 硫酸铜溶液能与铁反应,用于湿法炼铜 | |
| C. | 熟石灰具有碱性,和化肥硫酸铵混合使用改良酸性土壤 | |
| D. | 镁能在空气中燃烧发出耀眼的白光,可用于制造照明弹 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 上述反应共涉及三种氧化物 | |
| B. | 尿素含氮量高,是一种很好的氮肥 | |
| C. | C、H、0、N四种元素均位于周期表第二周期 | |
| D. | 尿素中含有CO分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
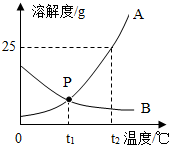 海洋中蕴含着丰富的资源,海洋资源开发前景十分广阔.
海洋中蕴含着丰富的资源,海洋资源开发前景十分广阔.
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生产豆芽使用速长王漂白剂,提高卖相 | |
| B. | 将氮气冲入食品包装袋中以防腐 | |
| C. | 使用铁锅,可预防缺铁性贫血 | |
| D. | 煲汤时放入适量的加碘盐以调味 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com