
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加人稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 43.5 | 37.0 | 33.75 | 33.75 |
分析 (1)根据锌会与硫酸反应,铜不会与硫酸反应,反应剩余的物质是铜,然后计算铜的质量分数;
(2)根据第一次与第二次的反应情况可以看出每50g硫酸消耗锌的质量是43.5-37=6.5g,然后利用三四次的反应中固体不变确定,50g样品中锌的质量是
50g-33.75g=16.25g,从而计算出反应时硫酸的消耗量;
(3)根据测得数据记录表,第2次加入稀硫酸后剩余固体质量继续减少,说明第1次所加入的稀硫酸完全反应,根据此时反应消耗锌的质量,计算所加入稀硫酸中溶质硫酸的质量,即可求得所用稀硫酸的溶质质量分数.
解答 解:(1)锌会与硫酸反应,铜不会与硫酸反应,反应剩余的物质是铜,所以铜锌合金中铜的质量分数为:$\frac{33.75g}{50g}$×100%=67.5%;
(2)由表中提供的数据可知该样品中含有的锌的质量=50g-33.75g=16.25g,由第一次与第二次可以得到:每50g硫酸消耗锌的质量是43.5-37=6.5g,所以反应的锌的质量是16.25g时,消耗的硫酸的质量是100g+25g=125g;
(3)依据题意,第一次中参加反应的锌的质量为50g-43.5g=6.5g,设参加反应的H2SO4质量为x
Zn+H2SO4=ZnSO4+H2↑
65 98
6.5g x
$\frac{65}{6.5g}$=$\frac{98}{x}$
x=9.8g
则所用稀硫酸的溶质质量分数=$\frac{9.8g}{50g}$×100%=19.6%.
故答案为:(1)67.5%;
(2)125;
(3)19.6%.
点评 利用实验数据中变化量的变化关系,分析反应的进行情况,对后面的计算时数据选择起着决定性作用;只有使用物质完全反应时的实验数据进行计算才能得到正确的结果.


科目:初中化学 来源: 题型:实验探究题
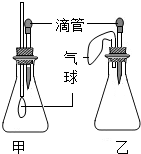 某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究.
某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究.| 实验操作 | 可能出现的现象与结论 | 同学评价 | |
| 第1组 | 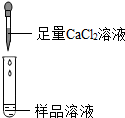 | 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是碳酸钠溶液呈碱性,也能使酚酞试液变红 |
| 第2组 | 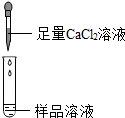 | 若产生白色沉淀,则猜想(1)不成立. | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立. |
| 第3组 | 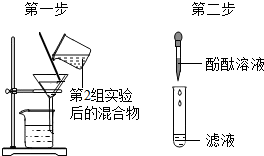 | 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立. | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是将第二组实验静置之后取上层清液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂 |
| A | NaNO3 | Na2CO3 | CaCl2 |
| B | ZnSO4 | CuSO4 | Zn粉 |
| C | Na2SO4 | NaHCO3 | HCl |
| D | CuO | Cu | H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
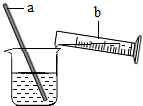 如图是稀释浓硫酸实验的示意图.
如图是稀释浓硫酸实验的示意图.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO | B. | CO2 | C. | O2 | D. | 什么气体都没有 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
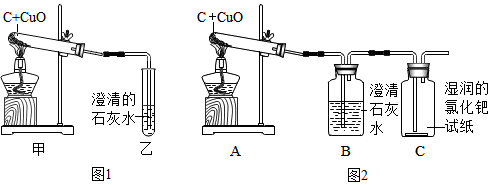
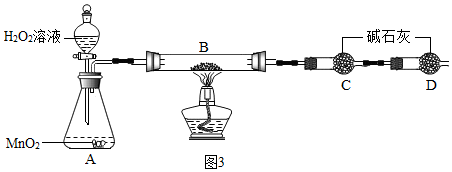
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
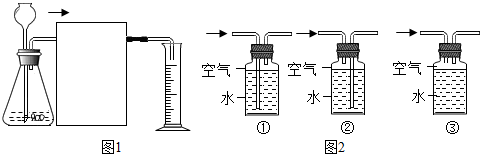
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
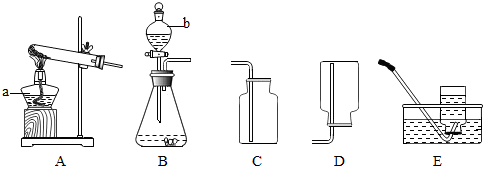
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com