
(3分)王老师要用含杂质质量分数为20%的大理石与足量的稀盐酸反应,制备10瓶二氧化碳气体。已知:①集气瓶的体积为100 mL;②大理石中杂质不与稀盐酸反应;③常温常压下二氧化碳的密度为1.98 g/L。
计算李王师需要准备大理石的最少质量。
5.625g
【解析】
试题分析:根据二氧化碳的体积和密度计算出二氧化碳的质量,再根据化学方程式中二氧化碳与碳酸钙的质量比,计算出碳酸钙的质量,再除以大理石中碳酸钙的质量分数即可求出大理石的质量。
解:反应生成的CO2质量=10×100ml×10-3L/ml×1.98g/L=1.98g
设参加反应的CaCO3质量为x
CaCO3 + 2HCl ="===" CaCl2 + CO2↑ + H2O
100 44
x 1.98 g
 =
=
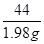
解得,x=4.5g
则需要准备大理石质量=4.5g÷(1-20%)=5.625g
答:需要准备大理石的最少质量为5.625g。
考点:根据化学反应方程式的计算
点评:解答本题的关键是要根据二氧化碳的体积和密度计算出质量,要注意体积、密度、质量的关系,还需要注意含杂质的质量。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2013届北京市延庆县九年级上学期期末考试化学试卷(带解析) 题型:计算题
(3分)王老师要用含杂质质量分数为20%的大理石与足量的稀盐酸反应,制备10瓶二氧化碳气体。已知:①集气瓶的体积为100 mL;②大理石中杂质不与稀盐酸反应;③常温常压下二氧化碳的密度为1.98 g/L。
计算李王师需要准备大理石的最少质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
王老师要用含杂质质量分数为20%的大理石与足量的稀盐酸反应,制备10瓶二氧化碳气体。已知:①集气瓶的体积为100 mL;②大理石中杂质不与稀盐酸反应;③常温常压下二氧化碳的密度为1.98 g/L。
计算李王师需要准备大理石的最少质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com