
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量氢氧化钠溶液于试管中,通入一定量二氧化碳后,再向溶液中滴加稀盐酸 | 有大量气泡冒出 | 二氧化碳与氢氧化钠发生了化学反应 |
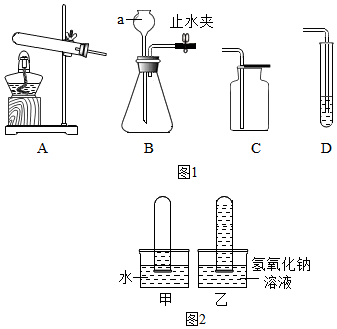
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据A装置制取氧气的反应物是固体,反应条件是加热,C装置收集氧气的方法是向上排空气法进行分析;
(3)①根据检查装置B的气密性的方法是:关闭止水夹,向长颈漏斗注入一定量的水,如果长颈漏斗中会形成一段稳定的水柱,说明装置气密性良好进行分析;
②根据二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色进行分析;
(4)①根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
②根据甲实验中液面的高度对比乙实验中液面的高度得出结论进行分析;
(5)根据溶液的碱性强弱与溶液中的氢氧根离子浓度有关进行分析;
(6)根据二氧化碳和碱反应会生成碳酸盐,碳酸盐和酸反应会生成二氧化碳气体进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是长颈漏斗;
(2)A装置制取氧气的反应物是固体,反应条件是加热,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,C装置收集氧气的方法是向上排空气法,原因是:氧气的密度比空气大;
(3)①检查装置B的气密性的方法是:关闭止水夹,向长颈漏斗注入一定量的水,如果长颈漏斗中会形成一段稳定的水柱,说明装置气密性良好;
②二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色,所以装置D中若盛放滴有紫色石蕊试液的水,可以观察到的现象是:紫色石蕊溶液变红色;若盛放氢氧化钠溶液,则没有明显现象产生;
(4)①氢氧化钠和二氧化碳反应生成碳酸钠和水,所以小明根据乙试管内的液体比甲试管内的液体高得多,判断二氧化碳和氢氧化钠发生了反应,化学方程式为:2NaOH+CO2=Na2CO3+H2O;
②甲实验中液面的高度对比乙实验中液面的高度得出结论,所以甲实验的目的是对比实验;
(5)溶液的碱性强弱与溶液中的氢氧根离子浓度有关,所以小菁取氢氧化钠溶液于烧杯中,用pH计测定溶液的pH为13.5.往溶液中通入二氧化碳一会儿,测得溶液的pH为11.2,继续通入二氧化碳,再测得溶液的pH为9.2,溶液的pH降低的原因是:溶液中氢氧化钠减少,溶液碱性减弱,该实验可以说明二氧化碳和氢氧化钠发生了反应;
(6)二氧化碳和碱反应会生成碳酸盐,碳酸盐和酸反应会生成二氧化碳气体,所以
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量氢氧化钠溶液于试管中,通入一定量二氧化碳后,再向溶液中滴加稀盐酸 | 有大量气泡冒出 | 二氧化碳与氢氧化钠发生了化学反应 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量氢氧化钠溶液于试管中,通入一定量二氧化碳后,再向溶液中滴加稀盐酸 | 有大量气泡冒出 |
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


科目:初中化学 来源: 题型:选择题
| A. | 钠应密封保存 | |
| B. | 钠与CO2的反应需在通风厨中进行 | |
| C. | 金属钠引起的着火可用二氧化碳灭火器灭火 | |
| D. | 钠与CO2反应生成的白色固体加水溶解后,滴加少量盐酸不会产生气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 合金材料的研究与工业生产的发展关系密切.
合金材料的研究与工业生产的发展关系密切.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验室用锌和稀硫酸反应制取氢气:Zn+H2SO4═ZnSO4+H2↑置换反应 | |
| B. | 酸雨形成中的反应:SO2+H2O═H2SO3 化合反应 | |
| C. | 用一氧化碳还原氧化铜:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2↑ 置换反应 | |
| D. | 溶洞中石笋的形成:Ca(HCO3)2═CaCO3↓+H2O+CO2↑ 分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 肥皂水 | 蔗糖水 | 食醋 | 柠檬汁 |
| pH | 10.2 | 7.0 | 3.3 | 2.0 |
| A. | 肥皂水 | B. | 蔗糖水 | C. | 食醋 | D. | 柠檬汁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com