
 纯碱样品中含有少量的氯化钠,某同学为测定纯碱样品中碳酸钠的含量,他取该纯碱样品12g,全部溶解在100g水中,再加入氯化钙溶液,所加氯化钙的质量如图所示.请计算:
纯碱样品中含有少量的氯化钠,某同学为测定纯碱样品中碳酸钠的含量,他取该纯碱样品12g,全部溶解在100g水中,再加入氯化钙溶液,所加氯化钙的质量如图所示.请计算:| 溶质的质量 |
| 溶液的质量 |
| 106 |
| 100 |
| x |
| 10g |
| 111 |
| y |
| 100 |
| 10g |
| 100 |
| 10g |
| 117 |
| z |
| 11.1g |
| 80.4g |
| 13.1g |
| 182.4g |


 寒假学与练系列答案
寒假学与练系列答案科目:初中化学 来源: 题型:
| A、鼓励使用太阳能热水器能有效减小雾霾 |
| B、化学在雾霾监测和治理中起重要作用 |
| C、大力发展火力发电能有效减小雾霾 |
| D、雾霾能使空气中可吸入颗粒物增多 |
查看答案和解析>>
科目:初中化学 来源: 题型:
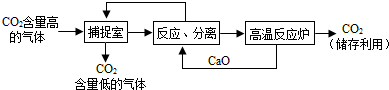
查看答案和解析>>
科目:初中化学 来源: 题型:
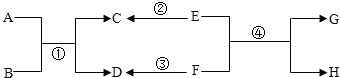 A、B、C、D、E、F、G、H之间的相互转化关系如图,它们均是初中化学中常见的物质,其中B、C是气体,且B是单质,E是含钠元素的化合物,G是一种常见的不溶于水的建筑材料.C、D在一定条件下也能反应生成A和B.
A、B、C、D、E、F、G、H之间的相互转化关系如图,它们均是初中化学中常见的物质,其中B、C是气体,且B是单质,E是含钠元素的化合物,G是一种常见的不溶于水的建筑材料.C、D在一定条件下也能反应生成A和B.查看答案和解析>>
科目:初中化学 来源: 题型:
| 名称 | 符号 | 原子结构示意图 | 单质化学式 | 常温常压下状态 | 单质与氢气反应 |
| 氟 | F | 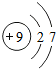 | F2 | 黑暗处爆炸 | |
| 氯 | Cl | Cl2 | 气态 | 光照爆炸 | |
| 溴 | Br |  | Br2 | 液态 | 加热反应 |
| 碘 | I |  | 固态 | 持续加热缓慢反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:
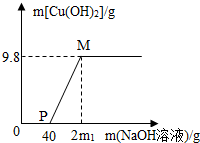 向含有CuCl2和HCl的混合溶液100g中,逐滴加入10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.
向含有CuCl2和HCl的混合溶液100g中,逐滴加入10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、0个 | B、1个 | C、2个 | D、3个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com