
【题目】化学实验室现有98%的浓硫酸,但在实验室中常需要用较稀的硫酸。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸,需要水的质量是多少?
【答案】195 g
【解析】
考点定位本题的考点是用水稀释改变浓度的方法。用水稀释改变浓度的方法就是指为了某种需要,向浓溶液中加入适量的水,将其稀释的所要求的浓度的方法,溶液稀释前后,溶质的质量是不变的。
解答过程由于溶液稀释前后,溶质的质量是不变的,故可根据溶质的质量不变进行我们先来找出稀释前后溶液、溶质、溶剂的变化:
溶质质量 溶剂质量 溶液质量 c%
加水前 50 g×98%=49 g 50 g-49 g=1 g 50 g 98%
加水后 49 g 1 g+x 50 g+x 20%
解:设需要水的质量为x
则 (50 g+x)×20%=50 g×98%
50 g+x=![]()
x=245 g-50 g
x=195 g
答:需加水195 g
试题总结评价:在解此类题时,首先要分析稀释前后哪个量不变,然后根据不变的量列出等量关系进行分析解答。


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
与“张牙舞爪”的雾霾相比,臭氧污染“隐藏”在万里晴空中,已成为夏季众多城市的大气环境污染元凶。
2019年3月29日,中国环境科学学会臭氧污染控制专业委员会成立。该领域的众多知名专家学者共同探讨大气臭氧污染防控的方向和路径。
臭氧(O3)原本是大气中自然产生的一种具有特殊臭味的微量气体,绝大部分臭氧存在于离地面25公里左右处的大气平流层中,这就是人们通常所说的臭氧层,它吸收对人体有害的短波紫外线,防止其到达地球。可它为何又是危害环境的污染物?
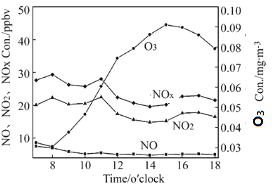
地表空气中的臭氧对人体极为有害,一些易于过敏的人长时间暴露在臭氧含量超过180微克/立方米的环境中,会产生眼睛刺痛,咳嗽等不良症状。研究表明,空气中每立方米臭氧含量增加100微克,人的呼吸功能就会减弱3%,对于运动员来说,空气中的臭氧含量可以直接影响到他们的耐力和比赛成绩。地表臭氧并不是人类活动直接排放出的污染物,而是因为氮氧化物或挥发性有机物与氧气结合而形成的,强烈的阳光照射会加速这一化学反应。氮氧化物主要来自于燃煤、汽车尾气等;挥发性有机污染物来源相对非常复杂,涂料、燃油、炼油厂、干洗店等,都会产生这种污染物。自2013年中国执行新《环境空气质量标准》,监测6种污染物以来,臭氧便成为一些城市夏季空气质量“超标日”的首要污染物,右图为某地臭氧、NO、NO2、NOX昼间12小时均值变化规律。
我国对于臭氧污染控制尚处于起步阶段,有效降低臭氧浓度依然任重而道远。
依据文章内容回答下列问题:
(1)从微观角度解释,氧气和臭氧化学性质不同的原因____不同。
(2)地表空气中的臭氧是由____生成的。
(3)如图,某地夏季某日昼时,臭氧污染最严重的时间段是____(填序号)。
A 8:00~10:00 B 10:00~12:00 C 12:00~14:00 D 14:00~16:00
(4)下列说法正确的是______(填序号)。
A 臭氧是一种无色无味气体
B 臭氧层具有吸收紫外线的作用
C 地表空气中臭氧的含量与天气阴晴无关
D 空气中臭氧浓度不同会对人体造成不同程度的影响
(5)为了减少臭氧污染,请你向市民提出一条可行建议_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列对应的化学方程式书写正确,且反应前后有元素化合价变化的是( )
A. 铁和盐酸混合制取氢气:2Fe+6HCl=2FeCl2+3H2↑
B. 生活中用天然气作燃料:C2H5OH+3O2![]() 2CO2+3H2O
2CO2+3H2O
C. 胃舒平(含氢氧化铝)治疗胃酸过多症:Al(OH)3+HCl=AlCl3+H2O
D. 赤铁矿(Fe2O3)高温下通CO炼铁:Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b、c三种固体物质(均不含结晶水)的溶解度曲线如图所示,请回答:
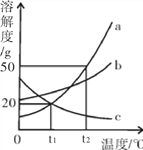
(1)t1℃时,三种物质的溶解度最大的是__________。
(2)t2℃时,将50 g固体a加入到50 g水中,充分搅拌后所得溶液的质量为_____g。
(3)将t2℃溶液质量相等的a、b、c三种物质的饱和溶液降温至t1℃,此时溶液的质量由大到小的顺序是________。
(4)下列有关说法正确的有_________。(填序号)
①其它条件不变,升高温度可使c的饱和溶液变成不饱和溶液
②t1℃时,a、c两种物质的饱和溶液中溶质的质量分数相等
③若a物质中混有少量b,可采用降温结晶的方法提纯a物质
④t2℃时,a、b、c三种物质配成的等质量饱和溶液中含溶剂质量最多的是a溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生产、生活息息相关,请你用化学知识回答以下生活中的问题:
(1)用洗洁精除去餐具上的油污,是由于洗洁精对油污有_____作用。
(2)生活中常用_____的方法降低水的硬度,同时又可以杀菌消毒。
(3)干冰常用来冷藏食品,是因为_____。
(4)人体摄入_____元素不足或过量均会引起甲状腺肿大。
(5)服用含氢氧化铝的药物治疗胃酸过多症,其化学方程式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】打造低碳、共享、智能、网联一体化的出行新生态,共享汽车逐渐普及,使人们的生活更加便利。

(1)“共享汽车”的塑料保险杠,属于_____材料,汽车的金属部分一般采用合金材料而不用纯金属的原因是_____。
(2)为防止车身的锈蚀,共享汽车所采用的方法是_____。
(3)汽车电路中的导线一般为铜芯线,这是利用金属铜良好的导电性和_____性。
(4)共享汽车用铅酸电池充电的反应: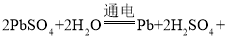 _____。共享汽车采用电力驱动,与传统汽车相比,大大减少了_____能源的消耗。
_____。共享汽车采用电力驱动,与传统汽车相比,大大减少了_____能源的消耗。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸中的H+没有被碱完全中和时生成的产物为酸式盐,可以继续和碱发生反应。同学们发现将一定量的NaOH溶液加入到NaHCO3溶液中,混合后无明显现象,如何证明两种物质发生了化学反应?反应后溶质有哪些?化学实验社的同学进行了下列探究:
(查阅资料)![]()
(实验探究1)用一定溶质质量分数的(NaHCO3,Na2CO3)溶液进行如下实验
|
| |
加稀盐酸 | A | 产生气泡 |
加无色酚酞溶液 | 溶液变红色 | 溶液变红色 |
加CaCl2溶液 | 无明显现象 | B |
上还表格中A处的实验现象为_____造成B处实验现象的原因是_____(用化学方程式表示)。
(猜想与假设)同学们对反应后溶液中溶质的成分进行了猜想
猜想1:![]()
猜想2:![]() 和
和![]()
猜想3:N![]() 和
和![]()
(实验探究2)
实验步骤 | 实验现象 | 实验结论 |
①取反应后溶液少许于试管中,请加过量的 | _____ | ①猜想2正确 ② |
②过滤后向滤液中加2﹣3滴无色酚酞试液 | _____ | |
③再滴加少量的_____ | _____ |
(表达与交流)对于没有明显现象的化学反应,可以通过检验有新物质生成或检验_____的方法来证明反应发生了。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】由两种金属组成的混合物共40g,与足量稀盐酸充分反应后,共放出2g氢气。则原混合物的组成不可能是( )
A. Zn和FeB. Fe和MgC. Zn和MgD. Al和Cu
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】市场上出售一种洗涤剂(标签如图),能瞬间清除衣服上汗渍、果汁渍等多种顽固污渍。某探究小组带着浓厚兴趣对这种洗涤剂的去污原理进行探究。

(査阅资料)
①过氧碳酸钠(Na2CO4)是白色晶体颗粒,常温下性质稳定,温度高于50℃时会分解,溶于水得到的溶液显碱性,与水反应会产生碳酸钠及其他化合物。
②碳酸钠具有去污能力,但不能清除衣物上的顽固污渍。
实验一:“溶解”样品
取适量该洗涤剂样品于锥形瓶中,加入适量蒸馏水,塞上带导管的橡皮塞,充分振荡,有气泡冒出,最终形成无色溶液a。将产生的气体通入石灰水,不变浑浊,打开橡皮塞,____(填操作),出现________现象,说明资料①中的“其他化合物”会产生氧气。
(提出问题)过氧碳酸钠与水反应产生的“其它化合物”是什么?
(猜想假设)
猜想1:H2O2
猜想2:NaOH
猜想3:H2O2、NaOH
实验二:验证产物
序号 | 实验操作 | 实验现象 | 分析与结论 |
(1) | 取适量溶液 a 于烧杯中,迅速加入稍过量的硝酸钡溶液,静置得清液 b。 | 产生白色沉淀 | 加入稍过量硝酸钡溶液,目的除去溶液中的碳酸钠。反应方程式为________。 |
(2) | 取少量清液 b 于试管中,加入少量二氧化锰。 | ________ | 反应的化学方程式是:____,证明过氧碳酸钠与水反应有H2O2 产生。 |
(3) | 再取少量清液 b 于试管中,滴加 2 ~3 滴氯化镁溶液。 | 无明显现象 | ________ |
(4) | 往含有酚酞的少量氢氧化钠稀溶液中,滴入 2 ~3 滴清液b。 | 有气泡产生, ________ | 过氧化氢在强碱性条件下易分解,且具有漂白性。 |
(实验结论)猜想________正确,写出过氧碳酸钠与水反应的化学方程式________。
(反思评价)该洗涤剂应________保存。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com