
“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用的工艺和技术。最近有科学家提出“绿色自由”构想:把CO2含量高的气体吹入饱和K2CO3溶液中,生成KHCO3,然后利用KHCO3受热易分解的性质,再把CO2提取出来,经化学反应使之变为甲醇(CH3OH)和水。“绿色自由”构想的技术流程如右图:(注:分解池内的反应条件是加热;合成塔内的反应条件为300℃、200kPa和催化剂)
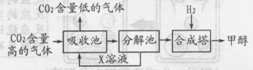
(1)合成塔内反应的化学方程式为_____________________________;
(2)X溶液可循环利用,溶质是___________(填写化学式)。
(1)3H2+CO2 300℃ 、200kPa 、催化剂 H2O+CH3OH (2)K2CO3
【解析】
试题分析:(1)根据题意,结合图示可知,合成塔内的反应是:氢气与二氧化碳反应,生成甲醇和水,反应条件是300℃、200kPa和催化剂,故反应的化学方程式为3H2+CO2 300℃ 、200kPa 、催化剂 H2O+CH3OH。
(2)根据题意,结合图示中由分解池分解后所得溶液X可通入吸收池再利用,可以确定其主要成分是碳酸钾,故化学式为K2CO3。
考点:物质的相互转化和制备,书写化学方程式、化学式
点评:解题时要学会根据流程图明确物质的制备过程,从而确定发生的化学反应,进而写出反应的化学方程式。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
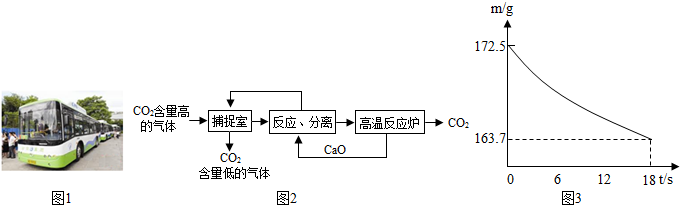
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| 工业纯碱标准:(Na2CO3%≥) | ||
| 优等品 | 一等品 | 合格品 |
| 99.2% | 98.8% | 98.0% |
查看答案和解析>>
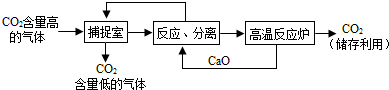
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com