
【题目】如图是甲、乙、丙三种物质在水中的溶解度曲线.

(1)t2℃时,甲的溶解度为________;
(2)t3℃时,等质量甲、乙、丙的饱和溶液降温到t2℃,所得溶液质量的大小关系是_________________;
(3)t1℃时,丙的饱和溶液中含有少量的甲,现要提纯丙并得到丙的固体,可以采用的操作方法是______________________;
(4)下列说法正确的是___________.
A 将甲、乙、丙的溶液分别从t1℃升温到t2℃,不考虑水分的蒸发,则溶质质量分数可能都不变
B t2℃时,向100g甲的饱和溶液中加入100g水,充分搅拌后溶质质量分数为10%
C t3℃时,等质量的甲、乙、丙分别制成饱和溶液,需要水的质量最多的是丙
D t2℃时,升高丙溶液的温度,一定有晶体析出.
【答案】25g 丙>乙>甲 升温结晶,马上(趁热)过滤 ABC
【解析】
(1)由图可知,t2℃时,甲的溶解度为25g;
(2)由图可知,甲乙物质的溶解度随温度的升高而升高,丙物质的溶解度随温度的升高而降低,t3℃时,等质量甲、乙、丙的饱和溶液降温到t2℃,丙变为不饱和溶液,甲乙都有晶体析出,且甲比乙析出的晶体多,故所得溶液质量的大小关系是丙>乙>甲。
(3)由溶解度曲线可知,甲的溶解度随温度的升高而升高,丙的溶解度随温度的升高而降低,故升温结晶,马上(趁热)过滤。
(4)A、当三种物质的不饱和溶液从t1℃升温到t2℃,不考虑水分的蒸发,则溶质质量分数都不变,故A选项正确;
B、t2℃时甲 物质的溶解度是25g,故100g甲的饱和溶液中含有甲物质的质量为:100g×![]() =20g,在加入100g 的水后,溶质质量分数为:
=20g,在加入100g 的水后,溶质质量分数为:![]() ×100%=10%,故B选项正确;
×100%=10%,故B选项正确;
C、t3℃时,甲乙丙的溶解度大小关系为甲>乙>丙,故等质量的甲、乙、丙分别制成饱和溶液,需要水的质量最多的是丙,故C选项正确;
D、t2℃时,升高丙的饱和溶液的温度,一定有晶体析出,故D选项错误。故选ABC。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:
【题目】某化学兴趣小组用如图装置验证一氧化碳还原氧化铜,并探究其还原产物的组成.

(1)装置及反应原理探究
①B装置中浓硫酸的作用为___________.
②说明CO能还原CuO的现象为___________
③上述整套装置中发生的化学反应,其中属于化合反应的化学方程式___________.(不考虑CO2和H2O的反应.)
(2)产物成分探究
[查阅资料]Ⅰ、一氧化碳还原氧化铜.除生成铜外还可能生成氧化亚铜(Cu2O)
Ⅱ、Cu2O为不溶于水的红色固体
Ⅲ、Cu2O+H2SO4═Cu SO4+Cu+H2O
[提出问题]红色固体含有什么物质?
[猜想假设]假设一:红色固体只含Cu
假设二:红色固体只含Cu2O
假设三:___________
[实验验证]该小组为验证上述假设,取少量红色固体,加到足量稀硫酸中,观察到溶液变为蓝色,红色固体部分溶解.
[实验结论]根据上述实验结果,可知红色固体中一定含有___________.
[数据处理]为进一步确定红色固体的成分,甲、乙两同不分别称取各自实验后的一定质量的红色固体,加到足量稀硫酸中使其充分反应,经过滤、洗涤、干燥后,称量剩余红色固体质量如表,请完善表中内容.
实验人员 | 红色固体(g) | 剩余红色固体(g) | 实验结论 |
甲 | 7.2 | 3.2 | ___________ |
乙 | 4.08 | 2.48 | ___________ |
[交流与反思]只要假设合理,方法正确,根据实验现象和数据就能得出结论.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取氯化钠和碳酸钠的混合物10.6克于烧杯中,完全溶解于一定量的水中,向所得溶液中滴加10%的稀盐酸,所加稀盐酸与生成气体质量如图所示,求:

(1)写出图中A点表示的溶质的化学式_______。
(2)图中BC段表示的意义是________。
(3)原混合物中碳酸钠的质量分数____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如下图所示:( “→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)
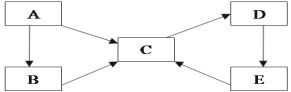
(1)若A、C的组成元素相同,且常温下都是液体。D为一种常见的碱,则C为____(填化学式);A→C的化学反应基本类型为___反应。
(2)若A为一种黑色固体,B、C的组成元素相同,D为一种常见的盐,则C为______(填名称);写出D→E的化学反应方程式_____。(任写一种)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酱油在使用及储藏过程中颜色会变深,逐渐降低品质。实验小组通过实验研究温度、氧气、光照3个因素对酱油颜色的影响。
(查阅资料)① 通过色差仪检测L*值可监控酱油颜色变化,酱油颜色越深,L*值越小。
② 保鲜瓶具有的特点是挤出盛放的物质后,空气不会进入。
(实验准备)
将等量样品(同品牌、同批次、初始L*值为43.82的酱油)分装到500 mL的不同容器中,密封。
(进行实验)
实验1:将装有样品的多个透明玻璃瓶置于不同温度的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。
编号 | 温度 | 15天 | 30天 | 45天 |
1-1 | 5 ℃ | 43.77 | 43.53 | 42.91 |
1-2 | 28 ℃ | 43.71 | 43.19 | 42.85 |
1-3 | 45 ℃ | 43.67 | 42.55 | 40.89 |
实验2:将装有样品的两个容器置于28 ℃的恒温箱中。每15天,分别倒出100 mL酱油,剩余样品放回恒温箱。用色差仪检测倒出样品的L*值,结果如下。
编号 | 容器 | 15天 | 30天 | 45天 |
2-1 | 透明玻璃瓶 | 43.45 | 42.36 | 41.30 |
2-2 | 透明保鲜瓶 | 43.72 | 42.98 | 42.53 |
实验3:将装有样品的多个容器置于28 ℃的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。

(解释与结论)
(1)实验1得出的结论是_____。
(2)实验2的目的是_____。
(3)实验3欲研究光照对酱油颜色的影响,应选用的容器是_____。
(4)家庭常使用透明玻璃瓶盛放酱油。解释“在相同时间内,使用过的酱油比未开封的酱油颜色深”可依据的实验是_____(填编号)。
(反思与评价)
(5)结合本实验,你对使用或储藏酱油的建议是_____。
(6)酱油在酿造过程中,有时会产生过量的铵盐(如NH4Cl)影响酱油的口感。可用碳酸钠除去铵盐,原理如下,补全该反应的化学方程式。Na2CO3 + 2NH4Cl === 2NaCl + 2NH3↑ + H2O +_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图示可表示物质在一定条件下发生化学反应的过程,下列说法正确的是
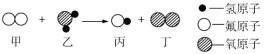
A. 该反应为置换反应B. 该反应中各物质都为化合物
C. 生成丙和丁的质量比为 4∶1D. 反应前后分子、原子个数都不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
“东风夜放花千树。更吹落、星如雨。”正如辛弃疾《青玉案·元夕》词中所描绘的一样,燃放烟花能制造出绚烂华丽的烟火,为节日增添喜庆气氛。
烟花爆竹发声、发光、发色的原理如下表所示。
主要原料及原理 | |
发声 | 烟火药主要成分是硝酸钾、硫磺、木炭等,点燃迅速产生大量的热和气体,引起爆炸。 |
发光 | 药剂中加入了铝、镁、铁等活泼金属粉末,在空中剧烈燃烧,发出耀眼强光。 |
发色 | 药剂中加入了一些金属盐类。这些金属元素在灼烧时会产生特殊颜色,例如,钠产生黄色,锶产生红色,钡产生绿色,铜产生蓝色等。 |
燃放烟花爆竹会导致大气污染和噪音污染。为打好“蓝天保卫战”,2018年开始,北京市制定了禁限放措施。除夕夜禁限放效果如下图所示。
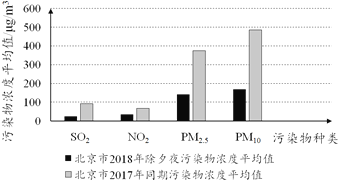
2008年北京奥运会开幕式上的烟花给人们留下了深刻的印象,其采用新型环保材料代替了纸壳,能在烟花起爆的瞬间充分燃尽;用压缩空气取代火药弹射礼花,实现“有光无污染、有响不爆炸”。冷焰火是选用燃点较低的金属粉末经过一定比例加工而成的冷光无烟焰火,安全性强、亮度高、烟雾小、环保无污染得到了大众的青睐。爱护环境,禁放烟花,从我做起。(数据选用的原文作者胡丙鑫等)
依据文章内容,回答下列问题。
(1)燃放烟花时,铁粉燃烧反应的化学方程式为______。
(2)发色原理中提到的钠、锶、钡、铜指的是______(填“单质”“元素”“原子”)。
(3)2018年除夕夜禁限放取得成效的依据是______。
(4)2008年北京奥运会新型烟花不产生大气污染的原因是______。
(5)下列关于烟花爆竹的说法正确的是______(填序号)。
A 药剂中加入钡盐燃放时可发出红光
B 冷烟火中的金属粉末燃点较低
C 发声原理是因为燃烧时产生大量的热和气体,引起的爆炸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示的四个图象,能正确反映对应变化关系的是( )
A.  水的电解
水的电解
B.  木炭在密闭的容器内燃烧
木炭在密闭的容器内燃烧
C.  加热一定量的高锰酸钾制氧气
加热一定量的高锰酸钾制氧气
D.  等质量的锌、铁与足量的稀硫酸反应
等质量的锌、铁与足量的稀硫酸反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com