
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
分析 根据表中提供的数据和反应的化学方程式可以进行相关方面的判断和计算.
解答 解:(1)第1次和第2次中,氯化钙溶液都是50g,样品质量不同,生成的沉淀质量相等,说明样品过量,第2次和第3次中,样品质量相等,氯化钙溶液质量不相等,产生沉淀质量相等,说明氯化钙溶液过量.
故填:3.
(2)设第3次过程中,碳酸钠质量为x,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100
x 4g
$\frac{106}{x}$=$\frac{100}{4g}$,
x=4.24g,
碳酸钠样品中杂质氯化钠的质量分数为:$\frac{5g-4.24g}{5g}$×100%=15.2%,
答:碳酸钠样品中杂质氯化钠的质量分数为15.2%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | XY | B. | XY2 | C. | X2Y | D. | X2Y3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2O | B. | CO2 | C. | N2 | D. | O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 原子核内有11个质子 | B. | 该元素属于非金属元素 | ||
| C. | 该原子失去电子后形成阳离子 | D. | 该原子核外有3个电子层 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
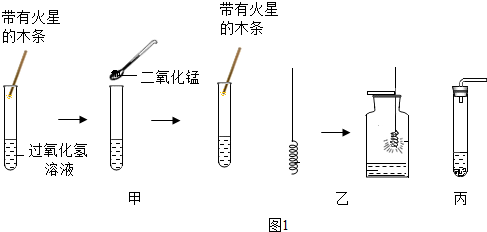
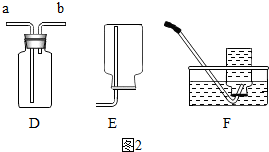
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com