3.
“氧泡泡”系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na
2CO
3•3H
2O
2).某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究.
【查阅资料】
Ⅰ.过碳酸钠在水中易离解成Na
2CO
3和H
2O
2,其水溶液具有Na
2CO
3和H
2O
2的双重性质;
Ⅱ.过碳酸钠与盐酸反应:2(2Na
2CO
3•3H
2O
2)+8HCl═8NaCl+4CO
2↑+3O
2↑+10H
2O;
Ⅲ.过碳酸钠的去污能力主要与其在反应中释放处的“活性氧”有关,“活性氧”含量越高,去污能力越强.
(1)20℃时,测得1%过碳酸钠水溶液的pH为10.5,说明其溶液呈碱性(选填“酸性”、“中性”或“碱性”).
(2)向过碳酸钠水溶液中加入少量MnO
2时产生大量气泡,发生反应的化学方程式是2H
2O
2$\frac{\underline{\;MnO_2\;}}{\;}$2H
2O+O
2↑.
(3)过碳酸钠样品中“活性氧”含量可按如下公式计算:
“活性氧”含量=$\frac{样品与足量盐酸反应生成的氧气质量}{样品质量}$×100%
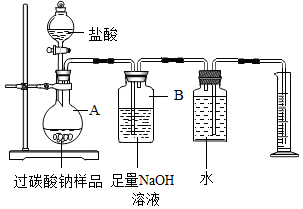
为测定某过碳酸钠样品中“活性氧”含量,取20g样品按如图实验装置与足量盐酸反应.(已知样品中杂质不溶于水且不与盐酸反应,装置气密性良好)
①将盐酸慢慢地入A中,反应一段时间,观察到没有气泡生成,停止滴加盐酸.
②装置B可吸收生成的CO
2,该反应的化学方程式是CO
2+2NaOH═Na
2CO
3+H
2O.
③甲同学认为若要得出生成氧气的质量,除要记录量筒内液体的读数外,还需要知道的数据是该实验条件下的密度.
④将反应后A中所得溶液过滤、蒸发、结晶、烘干,称得固体质量为11.7g,乙同学据此计算出该过碳酸钠样品的“活性氧”含量,写出其计算过程.
⑤完成上述探究后,丙同学提出:称量反应前后装置B的质量,其质量差就是反应生成CO
2的质量,据此可计算出样品中“活性氧”含量.但丁同学认为该方案不合理,丁同学的理由是盐酸挥发出的氯化氢气体进入到B中(填写一条即可)

 阅读快车系列答案
阅读快车系列答案 “氧泡泡”系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na2CO3•3H2O2).某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究.
“氧泡泡”系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na2CO3•3H2O2).某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究.