
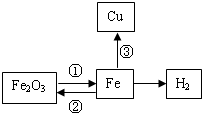
 构建知识网络是一种重要的学习方法.图为某校化学学习小组的小阳同学绘制的铁的化学性质网络示意图.请分析回答下列问题:
构建知识网络是一种重要的学习方法.图为某校化学学习小组的小阳同学绘制的铁的化学性质网络示意图.请分析回答下列问题: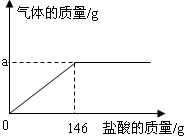
 2Fe+3CO2
2Fe+3CO2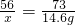
 ×100%=93.3%
×100%=93.3%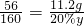 y=160g
y=160g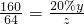 z=12.8g
z=12.8g 2Fe+3CO2,Fe+CuSO4═FeSO4+Cu;
2Fe+3CO2,Fe+CuSO4═FeSO4+Cu;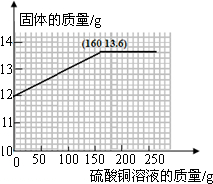


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
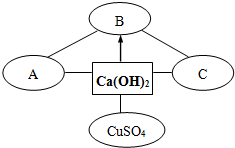 构建知识网络是一种重要的学习方法.如图是关于氢氧化钙化学性质的知识网络,“--”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,A、C分别属于氧化物及氯化物.完善这个知识网络:
构建知识网络是一种重要的学习方法.如图是关于氢氧化钙化学性质的知识网络,“--”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,A、C分别属于氧化物及氯化物.完善这个知识网络:查看答案和解析>>
科目:初中化学 来源: 题型:
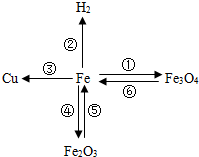 构建知识网络是一种重要的学习方法.如图是有关铁的性质和获得的网络图.
构建知识网络是一种重要的学习方法.如图是有关铁的性质和获得的网络图. ”均为铜片),只需完成实验
”均为铜片),只需完成实验
查看答案和解析>>
科目:初中化学 来源: 题型:
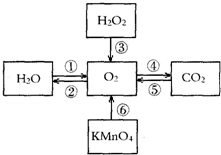 构建知识网络是一种重要的学习方法.如图是某同学构建的有关氧气获得和性质的网络图.请根据如图回答有关问题:
构建知识网络是一种重要的学习方法.如图是某同学构建的有关氧气获得和性质的网络图.请根据如图回答有关问题:查看答案和解析>>
科目:初中化学 来源: 题型:
 构建知识网络是一种重要的学习方法.将“分子”“原子”、“元素”填入如图序号所对应的横线上.
构建知识网络是一种重要的学习方法.将“分子”“原子”、“元素”填入如图序号所对应的横线上.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com