
【题目】曲酸(C6H6O4)是一种新型添加剂,它具有广泛的抗菌作用,作为防腐剂添加于食品中,具有非常好的效果.
(1)曲酸是由______种元素组成的。
(2)曲酸中碳、氢、氧三种元素的质量比是__________。
(3)曲酸中碳元素的质量分数是__________(精确到0.1%)
(4)284克的曲酸中含氧元素的质量是多少?________
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】下列化学方程式符合题意且书写正确的是( )
A. 不能用铁制容器配制波尔多液:2Fe+3CuSO4═Fe2(SO4)3+3Cu
B. 用点燃的方法除去二氧化碳气体中混有的少量一氧化碳:2CO+O2![]() 2CO2
2CO2
C. 验证Fe和Zn的金属活动性:Zn+FeCl2═ZnCl2+Fe
D. 铁丝在氧气中燃烧:4Fe+3O2![]() 2Fe2O3
2Fe2O3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从碳、氢、氧、氮、钙、铜六种元素中选择适当元素,用化学用语填空:
(1)两个钙离子 __________;
(2)属于碱的氮肥________;
(3)标出硝酸中氮元素的化合价 ________;
(4)厨房中常见的酸 _________;
(5)制消石灰的反应 ________________________;
(6)反应物都是氧化物且有二氧化碳生成的反应 ____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纳米级超细碳酸钙是一种新型超细固体材料,是橡胶、塑料制品、造纸、涂料、油墨等工业重要填料。工业上用石灰石来制备纳米级超细碳酸钙的流程如下图,请回答下列问题:

Ⅰ.煅烧炉中发生反应的化学方程式是 (28) 。操作1、2与实验室 (29) 操作类似。
Ⅱ.沉淀池中反应的基本类型属于 (30) 。石灰乳一般是在氧化钙中加水生成的,存在着还没有溶解的氢氧化钙,则石灰乳是 (31) (填:溶液、悬浊液、乳浊液)。
Ⅲ.上述流程中可循环使用的物质的化学式为 (32) 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线.
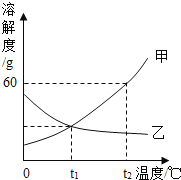
(1)溶解度随温度升高而减小的物质是________.
(2)t1℃时,甲、乙两种物质的溶解度______.
(3)要使乙的饱和溶液变为不饱和溶液,除加水之外还可采用的方法是_______.
(4)要使甲从其饱和溶液中析出,可用________的方法.
(5)t2℃时,甲的饱和溶液中溶质的质量分数是_________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图,回答问题:
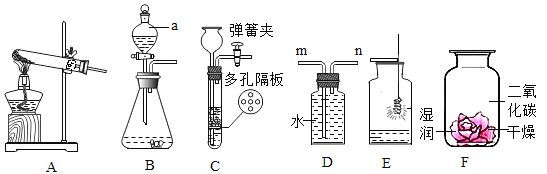
①仪器a的名称是_____。
②用氯酸钾和二氧化锰制取氧气。
(I)反应的化学方程式是______。
(II)用装置 D 收集氧气,则气体应从__________进(填“m”或“n”)。
(III)用装置 E 做“细铁丝在氧气中燃烧”的实验,未看到“剧烈燃烧,火星四射”现象, 可能的原因是_____(答出一条即可)。若实验成功,细铁 丝在氧气中燃烧的化学方程式____。
③用大理石与稀盐酸制取二氧化碳。
(I)发生装置可选用_____(在 A、B、C 中选)。
(II)一般不选用碳酸钠粉末替代大理石,原因是_____。
(III)如图 F 所示,探究二氧化碳与水反应时,将紫色石蕊试液浸泡过的小花,一半烘干放入盛有CO2的集气瓶中,观察到的现象是___________。其中干 燥的纸花要探究的问题是__________。
④欲测定③中稀盐酸的溶质质量分数。取 10g 溶质质量分数为 20%的氢氧化钠溶液,逐滴加入该盐酸,溶液的pH变化如右图所示。求:
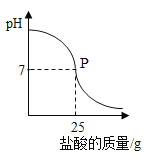
(I)P 点时,消耗氢氧化钠溶液中溶质的物质的量为__________mol。
(II)该稀盐酸的溶质质量分数。_______(根据化学方程式列式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙两个实验小组分别进行“加热硫酸铜和氢氧化钠溶液反应后生成物”的实验过程示意图
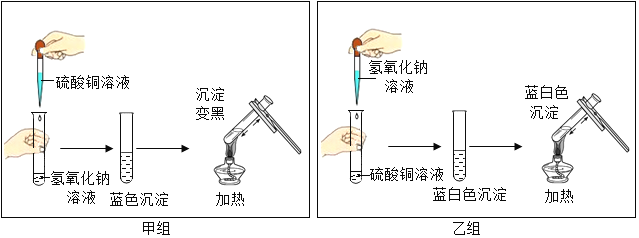
提出问题:影响氢氧化钠与硫酸铜反应产物的原因是什么?
查阅资料:
a.氢氧化铜为难溶于水的蓝色固体,受热易分解生成氧化铜和水
b.在一定条件下,氢氧化钠与硫酸铜在溶液中还可能发生如下反应:
![]() ,碱式硫酸铜是难溶于水的蓝白色固体,加热不易发生分解。
,碱式硫酸铜是难溶于水的蓝白色固体,加热不易发生分解。
①甲组:氢氧化钠与硫酸铜反应生成蓝色沉淀的化学方程式为_____。
②乙组与甲组实验结果不同的实验操作上的原因是_____。
③乙组同学反思并寻找与甲组实验的结果不同的真正原因。
一名同学想到,开始滴入氢氧化钠溶液时,没有沉淀产生,由此想到硫酸铜溶液是否显酸性,于是用pH试纸测定硫酸铜溶液的酸碱度,常温下测出其pH<7,则得出硫酸铜溶液呈_____性。
④实验反思:
甲、乙两组同学通过反复讨论,联想到了木炭燃烧,在反应物相同时,会有二氧化碳或一氧化碳不同产物出现,因此,对甲、乙两组出现不同实验现象做出的解释是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析。
(资料1)草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为H2C2O4·3H2O![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
(问题讨论)用下图所示装置进行实验:
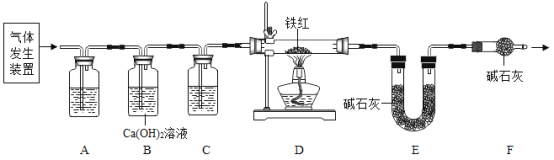
(1)实验前应先检查装置的气密性。
(2)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是_____(填字母编号)。
a 浓硫酸 b 澄清的石灰水 c 氢氧化钠溶液
(3)B装置的作用是________。
(4)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前将装置中的空气排出,防止发生爆炸。
②停止加热后_________。
(5)写出D装置中所发生反应的一个化学方程式____。
(数据分析与计算)
(资料2)铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
(6)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①D中充分反应后得到Fe粉的质量为mg。
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是_____。
(实验评价)
本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会____(填“偏小”、“不变”或“偏大”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图表示某些物质间转化关系(反应条件和部分产物已省略)。其中A、E为固体氧化物,且A为黑色粉末,E是红棕色固体;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属。请回答下列问题:
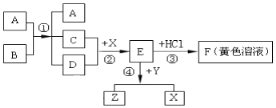
(1)反应①中A物质的作用是__________;
(2)反应③、④的化学方程式: ③________________;④__________________________;
(3)在日常生活中为防止反应②的发生,可采取的措施是______________(写一点即可);
(4)C的用途是_______________________(写一点即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com