
| 步骤 | 实验操作 | 预期现象与结论 |
| 1 | 分别在A、B两只试管中各加入2mL反应后的混合溶液 | |
| 2 | 向A试管中滴加几滴品红溶液,再滴入足量的稀硫酸 | 有气泡产生,品红溶液褪色, 证明含有Na2SO3. |
| 3 | 向B试管中,加入足量的氯化钡溶液 | 再加入稀盐酸 ,证明含有Na2SO4,则猜想3成立. |
分析 书写化学方程式时要注意配平;亚硫酸钠和稀盐酸反应能生成氯化钠、水和二氧化碳;
【进行猜想】
亚硫酸和氢氧化钠反应能生成亚硫酸钠和水,稀硫酸和氢氧化钠反应能生成硫酸钠和水;
【实验探究】亚硫酸钠和稀硫酸反应能生成硫酸钠、水和二氧化硫,二氧化硫能使品红溶液褪色;
氯化钡能和硫酸钠反应生成硫酸钡沉淀和氯化钠,硫酸钡不溶于稀硝酸;氯化钡能和亚硫酸钠反应生成亚硫酸钡沉淀和氯化钠,亚硫酸钡溶于稀硝酸,能和稀硝酸反应生成硝酸钡、水和二氧化硫;
【反思与交流】根据酸雨的形成解答即可.
解答 解:亚硫酸钡和稀盐酸反应能生成氯化钡、水和二氧化碳,反应的化学方程式为Ba2SO3+2HCl═BaCl2+H2O+SO2↑.
故填:BaSO3+2HCl=BaCl2+SO2↑+H2O;
【进行猜想】
如果酸雨中只含有亚硫酸,则盐是亚硫酸钠,如果酸雨中只含有硫酸,盐是硫酸钠,如果酸雨中含有亚硫酸和硫酸,则盐是亚硫酸钠和硫酸钠.
故填:只有Na2SO4.
【实验探究】
如果溶液中含有亚硫酸钠,向A试管中滴加足量的稀硫酸时,稀硫酸中和完过量的氢氧化钠后,和亚硫酸钠反应生成硫酸钠、水和二氧化硫,二氧化硫能使品红溶液褪色,观察到的实验现象是:有气泡产生,品红溶液褪色.
故填:有气泡产生,品红溶液褪色.
向B试管中,加入足量的氯化钡溶液,再加入足量的稀盐酸,如果先有白色沉淀,后有气体产生,沉淀部分溶解,证明含有亚硫酸钠和硫酸钠,因为加入足量的氯化钡溶液后,亚硫酸钠和氯化钡反应生成亚硫酸钡沉淀和氯化钠,硫酸钠和氯化钡反应生成硫酸钡沉淀和氯化钠,再加入足量的稀硝酸时,中和完氢氧化钠后,稀硝酸能和亚硫酸钡反应生成硝酸钡、水和二氧化硫,硫酸钡不能和稀硝酸反应.
故填:足量的氯化钡溶液;再加入稀硝酸;
【反思与交流】少用煤做燃料可以减少二氧化硫的排放,从而减少酸雨的形成,故填:少用煤做燃料.
点评 实验现象是反应的外在表现,通过实验现象可以判断化学反应的实质,要学会观察、分析实验现象,只有这样才能对问题作出正确的解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 钌-膦铬合物的质量在反应前后发生了变化 | |
| B. | 氢原子数在反应前后发生了改变 | |
| C. | 为CO2的利用创造了一种新途径 | |
| D. | 属于复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 单宁酸由碳、氢、氧三种元素组成 | |
| B. | 一个单宁酸分子中含26个氢分子 | |
| C. | 单宁酸属于有机物 | |
| D. | 一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验步骤 | 解释或化学方程式 | |
| 步骤1 | 实验前:CO必须经过验纯操作 | 因为CO具有可燃性,可能发生实验事故 |
| 步骤2 | 过程中,先通一段时间CO2再加热 | 这样做的目的是将玻璃管内的空气排尽,防止加热发生爆炸 |
| 步骤3 | 完全反应后,停止加热,继续通CO至室温 | 反应结束后,还要继续通CO至室温的目的是:防止金属氧化物被重新氧化A装置中发生的化学反应方程式有CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2(任写一个) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一氧化碳 | B. | 二氧化碳 | C. | 焦油 | D. | 烟灰 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
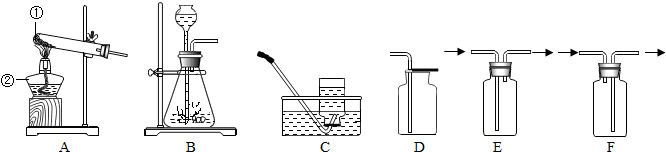
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 加入稀盐酸的质量/克 | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/克 | 8.25 | 6.5 | m | n | 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com