

| 抗胃酸药 | 复方氢氧化镁片 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
分析 (1)根据分子间有间隔分析判断回答;
(2)根据醋酸与盐酸一样,能与活泼金属反应生成氢气,醋酸与金属锌反应生成醋酸锌和氢气,写出反应的化学方程式即可.
(3)根据“过氧基”机构的特点分析判断;
(4)根据酸碱中和反应、氢离子与碳酸根离子反应等方面进行分析;
(5)首先要对模型图进行观察,分析物质的微观构成、物质的类别,再找出物质之间的微粒数目关系,然后再对题中各问加以分析解答;
解答 解:(1)物质的三态变化,主要是由于微粒的间隔发生了变化,微粒的大小和质量没有发生变化,微粒本身没有变化.
(2)由醋酸与氢氧化钠溶液反应生成醋酸钠和水的化学方程式为:CH3COOH+NaOH═CH3COONa+H2O可知,该反应的微观实质氢离子和氢氧根离子结合生成了水,即:H++OH-=H2O;醋酸与盐酸一样,能与活泼金属反应生成氢气,醋酸与金属锌反应生成醋酸锌和氢气,反应的化学方程式为:2CH3COOH+Zn=(CH3COO)2Zn+H2↑.
(3)由“过氧基”的结构特点可知,可用作杀菌消毒剂的是④.
(4)铝碳酸镁的氢氧根离子能与氢离子结合生成了水,碳酸根离子能与氢离子结合生成了碳酸,碳酸易分解生成了二氧化碳和水,所以起抗酸作用的两种微粒分别是OH-、CO32-.
(5)根据反应前后分子变化的微观示意图和质量守恒定律可知,各物质反应的微粒个数关系如下图: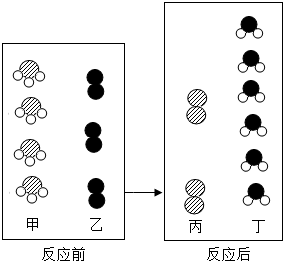
A、由图可知,反应前后一共有3种原子,故A错误;
B、由微粒的构成可知,该反应有单质生成,故B正确;
C、由微粒的变化可知,化学变化中分子可再分,但原子不可再分,故C错误;
D、由图可知,甲、丁两种分子的个数比是4:6=2:3,故D正确.
故答为:(1)D.(2)H++OH-=H2O;2CH3COOH+Zn=(CH3COO)2Zn+H2↑.(3)④.(4)OH-、CO32-.(5)BD.
点评 本题综合性较强,但由于问题较多,容易被弄糊涂了,因此要从概念的科学定义出发,逐一解答.不能光看图示,否则容易出错.


科目:初中化学 来源: 题型:选择题
| A. | 有盐和水生成的反应不一定是中和反应 | |
| B. | 由同种元素组成的物质不一定是单质 | |
| C. | 同种元素的原子和离子的质子数不一定相同 | |
| D. | 同一化合物中同种元素的化合价不一定相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如表:
为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如表:| 第I组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀硫酸的质量/g | 50 | 100 | 150 |
| 溶解固体的质量/g | 10.0 | 16.0 | 16.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中一定有银、肯定没有铜和锌 | |
| B. | 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 | |
| C. | 滤液中一定有硝酸锌、硝酸铜、硝酸银 | |
| D. | 滤渣中一定有银和锌,可能有铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 固体二氧化碳用于人工降雨 | B. | 稀有气体用于填充霓虹灯 | ||
| C. | 液氮用作制冷剂 | D. | 氧气用于医疗急救 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com