
分析 (1)水污染引起的藻类物质过渡的繁殖主要是因为水中溶有一些含有氮、磷、钾元素的物质;
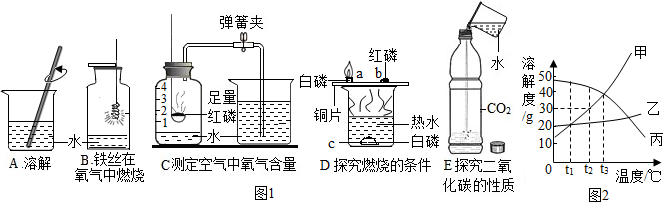
(2)①根据物质溶于水时,水做溶剂分析.
②根据铁丝在氧气中燃烧会产生大量的热使铁丝熔融溅落,瓶底的水能防止溅落的熔融的铁丝炸裂集气瓶分析.
③根据空气中的氧气约占空气体积的五分之一分析.
④根据白磷放在水中就和空气隔离分析.
⑤根据二氧化碳与水反应生成碳酸分析.
(3)利用质量守恒定律中元素的种类没有改变,原子的个数也没有增减的知识解决;
(4)①利用在t1℃时甲、乙、丙三种物质的溶解度曲线位置的上下关系,根据曲线在上方溶解度大,判断三种物质的溶解度大小;
②在t2℃时,甲、乙两物质的溶解度曲线交于一点,说明在t2℃时,两物质的溶解度相等;
③据t2℃时甲物质的溶解度为30g解答此题;
④根据溶解度的变化规律解答.
解答 解:
(1)受了污染的水能够使藻类物质过渡繁殖是因为水中溶有一些含氮、磷元素的物质,故答案为:C;
(2)
①物质溶于水时,水做溶剂,正确;
②铁丝在氧气中燃烧会产生大量的热使铁丝熔融溅落,瓶底的水能防止溅落的熔融的铁丝炸裂集气瓶,错误.
③空气中的氧气约占空气体积的五分之一,实验C中通过烧杯中水进入集气瓶中的体积可得出氧气约占空气总体积$\frac{1}{5}$的结论,正确;
④实验D中水的作用是提供热量和隔离空气,错误;
⑤二氧化碳与水反应生成了碳酸,实验E中的水仅作为反应物,正确.
(3)根据质量守恒定律,化学反应前后元素的种类不变,从化学方程式看,反应前有8个钾原子、4个铁原子和16个氧原子,反应后除aR外,有8个钾原子、10个氧原子,因此aR中有4个铁原子和6个氧原子,观察选项可知B正确;
(4)①t1℃时甲、乙、丙三种物质的溶解度曲线,丙的曲线在最上方,此时物质丙的溶解度最大;甲的曲线在最下方,此时物质甲的溶解度最小;因此,三种物质的溶解度由大到小的顺序为丙>甲>乙;
②在t2℃时,甲、乙两物质的溶解度曲线交于一点,说明在t2℃时,两物质的溶解度相等;
③据溶解度曲线知,t2℃时甲物质的溶解度为30g,即100g溶剂,溶解30g甲,故t2℃时,甲物质的饱和溶液中溶质与溶剂的质量比为30:100=3:10;
④别将t3℃时,甲、乙、丙的饱和溶液降温至t2℃时,甲和乙仍然是饱和溶液,由于甲的溶解度在t2℃时大于乙的溶解度,因此甲的溶质质量分数大于乙;丙无晶体析出,但在t2℃时丙中溶质最多,故所得的三种溶液中溶质的质量分数由大到小的顺序是丙>甲>乙.
答案:
(1)C;
(2)①③⑤;
(3)B;
(4)①丙>甲>乙;③相等;③3:10;④丙>甲>乙.
点评 本题考查了化学实验中水的不同用途,综合性强,有利于学生比较分析更牢固的掌握所学知识.溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
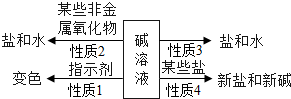 请结合小明同学对碱的四点化学性质的归纳图完成下列问题.(箭头上方的物质是指与碱反应的物质)
请结合小明同学对碱的四点化学性质的归纳图完成下列问题.(箭头上方的物质是指与碱反应的物质)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
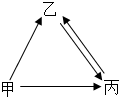 甲、乙、丙三种物质均含地壳中含量最多的元素.甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解生成丙;它们之间有如右图所示的转化关系(部分物质和反应条件已经略去).则:甲的化学式为H2O2;乙转化成丙的文字表达式为水$\stackrel{通电}{→}$氢气+氧气;从微观的角度解释甲、乙性质有差异的原因是分子构成不同.
甲、乙、丙三种物质均含地壳中含量最多的元素.甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解生成丙;它们之间有如右图所示的转化关系(部分物质和反应条件已经略去).则:甲的化学式为H2O2;乙转化成丙的文字表达式为水$\stackrel{通电}{→}$氢气+氧气;从微观的角度解释甲、乙性质有差异的原因是分子构成不同.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用盐酸区分锌片和银片 | B. | 用石蕊溶液区分稀硫酸和稀盐酸 | ||
| C. | 用水区分氢氧化钡和硫酸钡 | D. | 用水区分硝酸铵和氢氧化钠固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该反应属于置换反应 | |
| B. | 二氧化铈在反应前后质量和化学性质没有改变 | |
| C. | 二氧化铈中铈元素的化合价为+4 | |
| D. | 该反应的产物H2和CO均可作为气体燃料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com