
| A. | 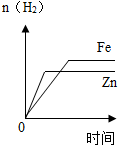 分别向质量相等的铁片和锌片中滴加过量的稀硫酸 | |
| B. | 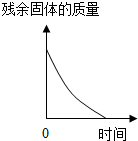 加热一定质量的高锰酸钾 | |
| C. |  某温度下,向一定质量的饱和硝酸钾中不断加入硝酸钾晶体 | |
| D. | 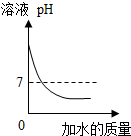 向一定质量的NaOH溶液中滴加水 |
分析 A、锌比铁活泼,相对原子质量比铁大;
B、高锰酸钾受热分解能生成锰酸钾、二氧化锰和氧气;
C、固体物质的溶解度决定于温度,饱和溶液则不会继续溶解溶质;
D、显碱性的溶液稀释时,碱性减弱.
解答 解:A、质量相等的铁片和锌片与稀硫酸反应时,锌与稀硫酸反应比铁与稀硫酸反应剧烈,完全反应需要的时间短;根据它们与稀硫酸反应的化学方程式可知,Zn→H2,Fe→H2,当铁片和锌片的质量相等时,铁与稀硫酸反应生成的氢气比锌与稀硫酸反应生成的氢气多,变化趋势与对应叙述关系正确.
B、加热一定质量的高锰酸钾时,随着反应的进行,剩余固体质量不断减小,但是不可能减小到零,因为反应中不断生成固体锰酸钾和二氧化锰,变化趋势与对应叙述关系不正确.
C、某温度下,向一定质量的饱和硝酸钾中不断加入硝酸钾晶体时,晶体不溶解,质量分数应该不变,变化趋势与对应叙述关系不正确.
D、氢氧化钠显碱性,稀释时,碱性减弱,pH减小,但是无论怎样稀释,溶液总是显碱性,pH不可能小于或等于7,变化趋势与对应叙述关系不正确.
故选:A.
点评 显酸性的溶液稀释时仍然显酸性,显碱性的溶液稀释时仍然显碱性,只不过是酸性或碱性的强弱变化罢了.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:解答题
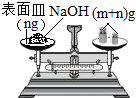 小明同学帮助老师配制500g质量分数为8%的氢氧化钠溶液,实验室现有:①托盘天平;②量筒;③烧杯;④玻璃棒;⑤酒精灯;⑥表面皿.请按要求回答下列问题:
小明同学帮助老师配制500g质量分数为8%的氢氧化钠溶液,实验室现有:①托盘天平;②量筒;③烧杯;④玻璃棒;⑤酒精灯;⑥表面皿.请按要求回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁粉用于制作照明弹 | B. | 氧化钙用作食品干燥剂 | ||
| C. | 钨用于制作白炽灯丝 | D. | 氮气用作焊接金属时的保护气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
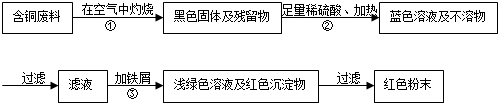
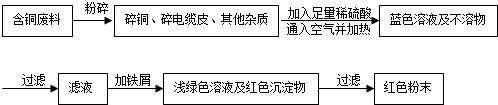
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 回忆教科书中有关“粗盐中难溶性杂质的去除”实验的主要步骤,回答有关问题:
回忆教科书中有关“粗盐中难溶性杂质的去除”实验的主要步骤,回答有关问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com