
| A. | 万一所住楼房失火,应立即开窗通风 | |
| B. | 误食重金属盐可先喝下大量鲜牛奶解毒 | |
| C. | 长期饮用蒸馏水不利于身体健康 | |
| D. | 燃煤使用脱硫技术可减少酸雨的形成 |
分析 A、根据促进物质燃烧的条件分析解答.
B、根据重金属盐可以使蛋白质变性来分析.
C、根据长期饮用纯净水,无法补充人体所需的微量的矿物质,进行分析判断.
D、根据燃煤脱硫后可以防止二氧化硫的产生进行分析判断.
解答 解:A、室内着火不应立即开窗通风,因为通风会进入更多的氧气,使燃烧更旺,故A错误,
B、重金属盐可以是蛋白质变性,所以误食后会中毒,服用大量的牛奶后,可以和重金属反应,变为不被吸收的物质,减弱对肠胃的影响,故B正确,
C、长期饮用纯净水,无法补充人体所需的微量的矿物质,不宜于身体健康,故C正确.
D、使用燃煤脱硫技术,减少酸雨的产生,故D正确.
故选A.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.


科目:初中化学 来源: 题型:推断题
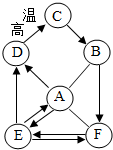 A、B、C、D、E、F均为初中化学中常见的物质,E俗称纯碱,它们之间存在如图的转化关系.“→”表示物质间存在着相应的转化关系,“-”表示物质间能发生反应(部分反应物、生成物和反应条件未标出).
A、B、C、D、E、F均为初中化学中常见的物质,E俗称纯碱,它们之间存在如图的转化关系.“→”表示物质间存在着相应的转化关系,“-”表示物质间能发生反应(部分反应物、生成物和反应条件未标出).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 试验编号 | 盐酸的质量分数/% | 反应温度 | 铝丝消失时间/s |
| ① | 3 | 20 | 500 |
| ② | 6 | 20 | 300 |
| ③ | 6 | 30 | 80 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 家庭中,提倡垃圾分离 | B. | 工作中,采取无纸化办公 | ||
| C. | 工业上,回收废旧金属再利用 | D. | 交通上,拓宽马路,鼓励私家车出行 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
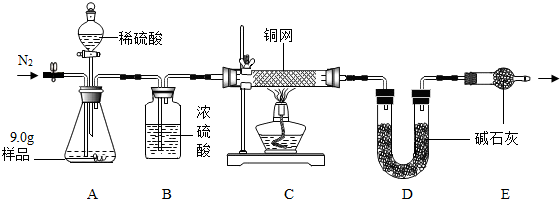
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1.5g | B. | 1.3g | C. | 2.0g | D. | 1.2g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
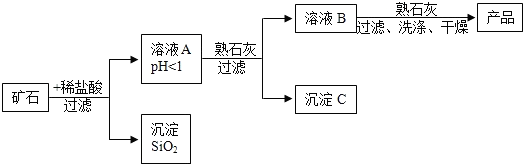
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 8.6 |
| 完全沉淀的pH | 3.2 | 6.7 | 11.1 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
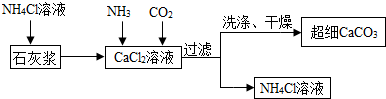
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com