
【题目】在高温下,铁与水蒸气能发生反应生成一种常见铁的氧化物和一种气体,某学习小组的同学对此反应很感兴趣,在小组集体协作下设计了如图实验,以探究铁粉与水蒸气反应后的产物,也邀请你一起来完成下列探究: 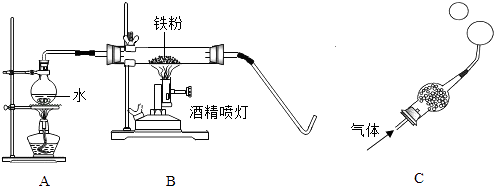
【猜想与假设】猜想一:生成的气体可能是氢气;猜想二:生成的气体可能是氧气.
【实验探究】将生成的气体通入C装置.球形管里装有碱石灰干燥剂.导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡.当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
(1)【推断】生成的气体是 .
(2)探究试管中剩余固体成分是什么? 【查阅资料】
Ⅰ.铁的氧化物①只有是Fe2O3红棕色,其余FeO、Fe3O4均为黑色;
②只有Fe3O4能被磁铁吸引.
Ⅱ.铁的氧化物都能与盐酸反应,但没有气体生成.
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是 .
(3)【实验探究】
实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量 | 无气泡产生,黑色固体是 |
(4)【实验结论】铁与水蒸气反应的化学方程式为: .
(5)【拓展延伸】Ⅰ.铁、镁混合物5.6g与足量稀硫酸反应,生成的氢气质量不可能是( )
A.0.2g
B.0.3g
C.0.4g
D.0.5g
(6)Ⅱ.某同学为探究铁合金中铁的质量分数,先后进行了四次实验(铁合金中除铁外,其余成分不与稀硫酸反应),实验数据如表.根据该同学的实验,试回答以下问题:
第一次 | 第二次 | 第三次 | 第四次 | |
所取合金的质量∕g | 10 | 10 | 20 | 30 |
所加稀硫酸的质量∕g | 100 | 120 | 80 | X |
生成氢气的质量∕g | 0.2 | 0.2 | 0.2 | Y |
表中第四次实验中,合金里的铁恰好与稀硫酸完全反应,则其中X=Y= .
(7)该铜铁合金中铁的质量分数是多少?(写出计算过程)
【答案】
(1)氢气
(2)Fe与Fe3O4
(3)稀盐酸;Fe3O4
(4)3Fe+4H2O ![]() Fe3O4+4H2
Fe3O4+4H2
(5)AD
(6)240;0.6
(7)解:设铁合金中铁的质量分数为x.
Fe+H2SO4=FeSO4+ | H2↑ |
56 | 2 |
30g×x | 0.6g |
![]()
x=56%
答:铁合金中铁的质量分数为56%。
【解析】解:【推断】用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体具有可燃性、密度小于空气,再根据反应物为“铁与水蒸气”,所以是氢气;【猜想与假设】能被磁铁吸引的只有Fe与Fe3O4 , 则猜想一Fe3O4;又不可能只有Fe没有其他反应产物,猜想二是Fe与Fe3O4;验证猜想一与猜想二,关键是否含有Fe. 【实验探究】根据铁与稀盐酸反应产生气体,进行设计实验:
实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量的稀盐酸 | 无气泡产生,黑色固体是Fe3O4 . |
【实验结论】根据“高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体”和猜想,所以铁和水蒸气反应会生成四氧化三铁和氢气,化学方程式为:3Fe+4H2O ![]() Fe3O4+4H2;
Fe3O4+4H2;
【拓展延伸】Ⅰ.假设5.6g全部是铁,则生成氢气的质量=5.6g× ![]() =0.2g;假设5.6g全部是镁,则生成氢气的质量=5.6g×
=0.2g;假设5.6g全部是镁,则生成氢气的质量=5.6g× ![]() =0.47g;所以铁粉、铝粉的混合物5.6g与足量的稀硫酸完全反应,则反应中生成氢气的质量范围是0.2g<氢气<0.47g;故选:AD.Ⅱ.一、二次实验相比说明10g合金与足量硫酸反应最多生成0.2g氢气;一、三次实验相比说明80g稀硫酸与足量合金反应最多生成0.2g氢气.即10g合金与80g稀硫酸恰好完全反应生成0.2g氢气.
=0.47g;所以铁粉、铝粉的混合物5.6g与足量的稀硫酸完全反应,则反应中生成氢气的质量范围是0.2g<氢气<0.47g;故选:AD.Ⅱ.一、二次实验相比说明10g合金与足量硫酸反应最多生成0.2g氢气;一、三次实验相比说明80g稀硫酸与足量合金反应最多生成0.2g氢气.即10g合金与80g稀硫酸恰好完全反应生成0.2g氢气.![]() ,解得X=240g;
,解得X=240g;![]() ,解得Y=0.6g.(7)设铁合金中铁的质量分数为x.
,解得Y=0.6g.(7)设铁合金中铁的质量分数为x.
Fe+H2SO4=FeSO4+ | H2↑ |
56 | 2 |
30g×x | 0.6g |
![]()
x=56%
答:①X 240g,Y 0.6;
②铁合金中铁的质量分数为56%.
所以答案是:
【推断】氢气;
【猜想与假设】猜想二:Fe与Fe3O4;
【实验探究】
实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量的稀盐酸 | 无气泡产生,黑色固体是Fe3O4 . |
【实验结论】3Fe+4H2O ![]() Fe3O4+4H2;
Fe3O4+4H2;
【拓展延伸】Ⅰ.AD.Ⅱ.①X 240,Y 0.6;②铁合金中铁的质量分数为56%.
【考点精析】关于本题考查的书写化学方程式、文字表达式、电离方程式和根据化学反应方程式的计算,需要了解注意:a、配平 b、条件 c、箭号;各物质间质量比=系数×相对分子质量之比才能得出正确答案.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】现有工厂丢弃的废铜屑(铜屑表面呈绿色).课外活动小组同学欲利用其制取硫酸铜晶体,他们设计了下面的两种制取流程(如图1).请回答: 
(1)铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3 , 从组成分析,预测它除了能与稀硫酸反应后,还能与(任举一例)反应.操作①所用的玻璃仪器有烧杯、玻璃棒和;溶液A的溶质有;两种方法得到硫酸铜晶体,你觉得符合绿色化学要求的方法是 .
(2)方法二的化学反应的化学方程式为2Cu+2H2SO4+ ![]() 2CuSO4+ .
2CuSO4+ .
(3)硫酸铜晶体广泛应用在电镀、印染、农药等方面,波尔多液是一种农业常用杀菌剂,它由硫酸铜、生石灰加水配制而成,不能用铁制容器来配制波尔多液的原因是(用化学方程式表示) , 此反应属于基本反应类型中的反应.
(4)理论上废铜屑中的铜完全可以转化为硫酸铜.已知废铜屑的质量为100kg,若最后所得的硫酸铜质量为80kg,则废铜屑中铜的质量分数为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】建湖是美丽水乡,请回答下列问题:
(1)含有较多可溶性钙、镁化合物的水叫做(填“软水”或“硬水”).
(2)实验室用自来水制取蒸馏水的蒸馏烧瓶里,通常要加入几粒碎瓷片.碎瓷片的作用是 .
(3)浓硝酸在光照条件下发生反应,除了生成水和氧气外,还有X,化学方程式为4HNO3 ![]() 4X↑+O2↑+2H2O,X的化学式为 .
4X↑+O2↑+2H2O,X的化学式为 .
(4)如图为A、B、C三种物质的溶解度曲线: 
①t1℃ 时,向100g水中加入20gA物质,充分搅拌后,所得溶液的质量是
g.
②若A中含有少量B,可用的方法提纯A.
③压强为101kPa,N2的溶解度曲线与(填A、B或C)的溶解度曲线最为相似.
④将C物质的不饱和溶液变为饱和溶液,下列说法正确的是(填字母).
a,溶液中溶质的质量一定增加b,溶液中水的质量一定减少c,溶液的质量可能不变.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】N(NO2)3是科学家2011年发现的一种新型火箭推进剂的原料.下列有关说法正确的是( )
A.N(NO2)3由三种元素组成的化合物
B.一个N(NO2)3分子中氮、氧原子个数比为4:5
C.N(NO2)3的相对分子质量152 g
D.N(NO2)3中氮元素的质量分数表达式 ![]() ×100%
×100%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com