
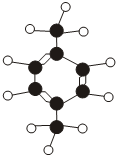
 4月6日,福建古雷石化(PX项目)厂区发生爆炸,经过消防官兵几天的奋战,成功扑灭大火.PX是一种重要的化工原料,从化纤织物到食品包装,从医疗设备到家用电器,都要用到它的合成产物.PX的化学名称为对二甲苯,是一种低毒化合物,
4月6日,福建古雷石化(PX项目)厂区发生爆炸,经过消防官兵几天的奋战,成功扑灭大火.PX是一种重要的化工原料,从化纤织物到食品包装,从医疗设备到家用电器,都要用到它的合成产物.PX的化学名称为对二甲苯,是一种低毒化合物, ”代表碳原子.“
”代表碳原子.“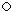 ”代表氢原子.试根据分子模型写出对二甲苯的化学式C8H10.
”代表氢原子.试根据分子模型写出对二甲苯的化学式C8H10.分析 (1)根据物质的分子构成情况来分析其化学式;
(2)根据相对分子质量为组成分子的各原子的相对原子质量之和,根据化合物中元素的质量比等于相对原子质量与原子个数的乘积之比来分析;元素质量分数的计算方法来分析;
(3)根据题干中的信息来进行分析解答.
解答 解:(1)由二甲苯的分子结构模型可以书写出它的化学式为:C8H10;故填:C8H10;
(2)其相对分子质量为12×8+1×10=106,对二甲苯中,碳、氢元素的质量比为(12×8):(1×10)=48:5,其中碳元素的质量分数为:$\frac{12×8}{12×8+1×10}×100%$=90.6%;故填:106;48:5;90.6%;
(3)A.由题干中的信息可知,PX在生产中的应用是非常广泛的,所以在符合环保的条件下,要适度发展PX项目,错误;
B.有题干信息可知,正确;
C.虽然PX项目存在一定的污染,但是可以通过治理加以克服,错误.
故选:B.
点评 本题考查了社会发展过程中,化学物质在其中扮演的角色,从总体上看,化学物质在社会发展中起到了重要的作用,但是也带来了一系列环境污染方面的问题,要客观地分析化学物质的作用,既要重视它的作用,也要想法消除它的不利影响.


科目:初中化学 来源: 题型:填空题
 如何合理、高效、节约地使用煤、石油、天然气这三大当今世界最主要的化石燃料,加紧开发、研制其它清洁能源是全人类面临的共同课题,是发展低碳经济的当务之急.回答下列问题:
如何合理、高效、节约地使用煤、石油、天然气这三大当今世界最主要的化石燃料,加紧开发、研制其它清洁能源是全人类面临的共同课题,是发展低碳经济的当务之急.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
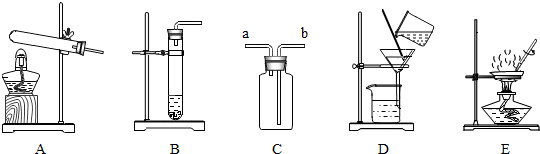
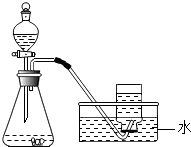 下列制取和收集气体的方案,可以直接采用如图所示装置进行的是CD
下列制取和收集气体的方案,可以直接采用如图所示装置进行的是CD查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 步骤1:取少量过滤后的废液于试 管中,滴加溶液 | 溶液没有变红 | 废液的溶质中 不含FeCl3 |
| 步骤2:另取少量过滤后的废液于试管中,加入过量的Na2CO3溶液 | 猜想2成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 焚烧秸秆增加肥力 | B. | 城区严禁燃放烟花爆竹 | ||
| C. | 大力发展电力公交 | D. | 关闭燃煤小锅炉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com