
分析 HAc属于酸类,具有酸的通性,能使石蕊变红,因为醋酸具有挥发性故存放时要密封保存,通过盐酸与纯碱的反应,可类比HCl写出Na2CO3与Hac反应的第一步化学方程式.
解答 解:(1)醋酸属于酸,具有酸的共性,能使紫色石蕊变红,故答案为:红.
(2)因为醋酸与盐酸都具有较强挥发性,故存放应该密封,故答案为:密封.
(3)利用醋酸与纯碱反应方程式的书写,类比可写化学方程式,故答案为:Na2CO3 +HAc═NaHCO3 +NaAc.
(4)因为醋酸具有较强的挥发性,加热会使其全部蒸发掉,所以程明的说法错误,故答案为:小刚,由于HAc具有挥发性,在蒸发过程中已经挥发掉.
点评 此题是对醋酸知识的考查,解题的关键主要是利用类比的方式对要求进行分析,再通过相关所学知识进行解决.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
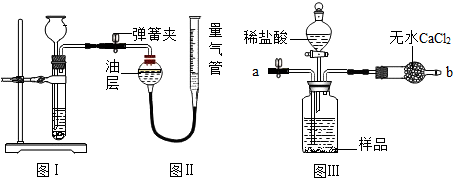
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
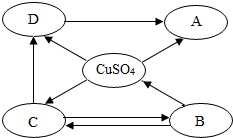 构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:
构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 化学式 | A | B | C | D |
| 反应前质量(g) | 28 | 102 | 4 | 4 |
| 反应后质量(g) | 0 | 6 | 92 | 未知 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
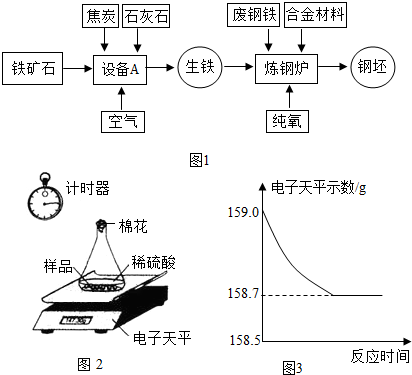
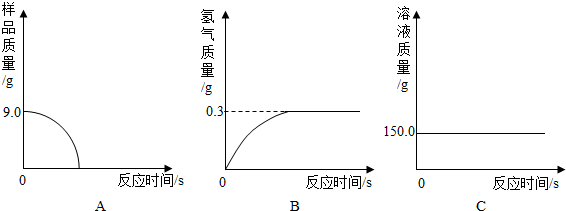
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com