
| A. | NaOH | B. | CO2 | C. | HCl | D. | Na2CO3 |
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 室内插花,满室飘香,说明分子不断运动的反映 | |
| B. | 热胀冷缩,说明分子的大小可随温度的改变而改变 | |
| C. | 10mL酒精和10mL水混合后,体积小于20mL,说明分子之间有间隔 | |
| D. | 湿衣服放在火炉旁,干得较快,说明分子运动速率随温度升高而加快 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 酸碱盐是有广泛用途的重要化合物,某化学活动小组的同学围绕这几类化物合进行了一系探究活动.
酸碱盐是有广泛用途的重要化合物,某化学活动小组的同学围绕这几类化物合进行了一系探究活动.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 相关说法 | 解 释 |
| A | 碳酸氢钠受热易分解而碳酸钠受热不易分解 | 不同种物质的分子性质不同 |
| B | 氯化钠溶液能导电 | 溶液中存在自由移动的粒子 |
| C | 水银温度计温度升高时,液柱上升 | 温度升高,分子间间隔增大 |
| D | 有机物数目异常庞大 | 原子的排列方式不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
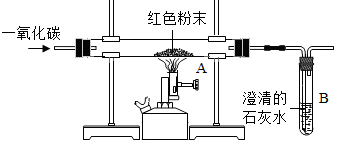 如图是课本中模拟炼铁的实验装置.
如图是课本中模拟炼铁的实验装置.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
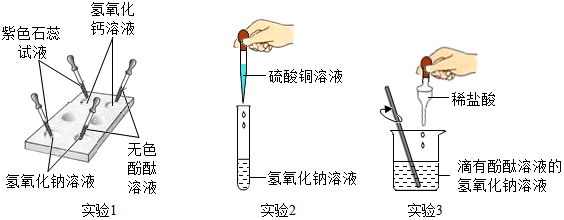
| 实验步骤 | 预计现象及相应结论 |
| 取2支洁净的试管,分别加入等体积的两种待测溶液,再分别滴加相同滴数的无色酚酞试液,向溶液中滴加10%的稀盐酸,计算红色刚好消失时所滴加稀盐酸的滴数(或用量) | 红色刚好消失时所滴加稀盐酸的滴数少的为5%的氢氧化钠溶液,另一种为10%的氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 1 | 20 | 15 |
| 2 | 20 | 10 |
| 3 | 20 | 6.8 |
| 4 | 20 | n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com