
分析 此题是对质量守恒定律相关应用的考查,由氯酸钾制取氧气的反应可知,反应前氯酸钾的质量应该等于氯化钾和氧气的质量之和,据此并依据催化加的特点分析解答即可.
解答 解:根据质量守恒定律:氧气的质量=24.5g+2g-16.9g=9.6g;
设氯化钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 9.6g
$\frac{149}{96}$=$\frac{x}{9.6g}$,解得x=14.9g;
故答案为:9.6;14.9.
点评 此题是对质量守恒定律的应用考查,解题的关键是掌握有关催化剂的意义以及相关的化学反应特点.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:初中化学 来源: 题型:选择题
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | 2FeCl2+Cl2=2FeCl3 | ||
| C. | Na2SiO3+H2SO4=H2SiO3↓+Na2SO4 | D. | 4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2N2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  合理使用化肥为粮食的丰收保驾护航 | |
| B. |  使用钢材、水泥等材料复建哈尔滨火车站 | |
| C. |  明年冰城学生免费使用教科书 | |
| D. |  提供燃料,实现国人的飞天梦想 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该变化是物理变化 | |
| B. | 臭氧与氧气是同一种物质 | |
| C. | 该变化是化学变化 | |
| D. | 氧气能转化为臭氧,是氧气的物理性质 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 它是一种新型的化合物 | B. | 它是一种单质 | ||
| C. | 它的一个分子中有8个硫原子 | D. | S8可以表示8个硫原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 明明将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会后,采用如图所示装置进行过滤,请问:
明明将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会后,采用如图所示装置进行过滤,请问:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
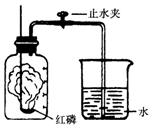 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | SO42-、Fe3+、Na+、OH- | B. | K+、SO42-、Cu2+、NO3- | ||
| C. | Cl-、K+、SO42-、OH- | D. | SO42-、Cl-、CO32-、Na+ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 1992年6月1日,中国人民银行发行了隶属第四套人民币的第三套金属流通币,面值为1角、5角、1元三枚,1元币为牡丹花图案,5角为梅花图案,1角为菊花图案.其中,梅花5角硬币是1980至1986年发行铜合金长城币(1、2、5角,1元)后,又一次发行的铜合金币,材质为黄铜,颜色金黄,设计、制作精良,美观大方,俗称“梅花5角”硬币.
1992年6月1日,中国人民银行发行了隶属第四套人民币的第三套金属流通币,面值为1角、5角、1元三枚,1元币为牡丹花图案,5角为梅花图案,1角为菊花图案.其中,梅花5角硬币是1980至1986年发行铜合金长城币(1、2、5角,1元)后,又一次发行的铜合金币,材质为黄铜,颜色金黄,设计、制作精良,美观大方,俗称“梅花5角”硬币.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com