
 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
分析 (1)根据加入足量的BaCl2溶液,产生白色沉淀,该白色沉淀是BaCO3,说明该固体成分中含有CO32-;再加入CuSO4溶液,产生蓝色絮状沉淀,该蓝色絮状沉淀是Cu(OH)2,说明该固体成分中含有OH-进行分析;
(2)根据质量守恒定律可以知道反应前后减少的质量为生成的二氧化碳的质量;根据生成的二氧化碳的质量结合反应的化学方程式可以求算出碳酸钠的质量,并求算出碳酸钠的质量分数;
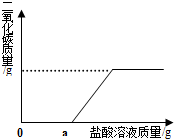
(3)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,而图中曲线所示,开始加入稀盐酸时并没有气体产生,可判断此时盐酸没有和碳酸钠发生反应.
解答 解:(1)根据题意知,该固体溶液中含有CO32-和OH-,所以这瓶久置的氢氧化钠固体是NaOH和Na2CO3的混合物;
(2)根据质量守恒定律可以知道反应前后减少的质量为生成的二氧化碳的质量,其质量为:148.5g-146.3g=2.2g;
设样品中碳酸钠的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{x}$=$\frac{44}{2.2g}$
解得:x=5.3g
该样品中Na2CO3的质量分数为$\frac{5.3g}{10.6g}$×100%=50%;
答:该样品中Na2CO3的质量分数为50%;
(3)根据加入稀盐酸的质量与产生CO2气体的质量关系图可知,在一开始加入稀盐酸时并没有气体产生,说明此时所加稀盐酸与氢氧化钠发生反应.
故答案为:(1)NaOH和 Na2CO3的混合物;
(2)二氧化碳质量2.2克,碳酸钠质量分数50%;
(3)氢氧化钠.
点评 在解此类题时,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:初中化学 来源: 题型:选择题
| A. | 空气是由氮气和氧气组成的 | |
| B. | 呼出气体中氧气的含量比空气中的小 | |
| C. | 呼吸过程中消耗了空气 | |
| D. | 呼出的气体是二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 浓硫酸500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 强腐蚀性,阴冷,密封储藏 | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com