
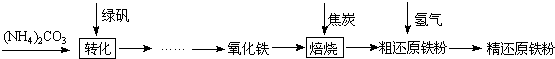

分析 (1)CO具有还原性,能与氧化铁反应而使氧化铁还原成铁,同时放出二氧化碳;
(2)焦炭燃烧放出大量的热,该热量可维持其它反应的发生;
(3)装置A在加热时发生反应,生成的水与甲烷通过装置B处理后进入装置C,进入该装置的气体在加热条件下发生反应;
(4)步骤③的目的是 除去装置内的氧气,防止发生爆炸,验证该步骤目的达到的实验方法是收集尾气靠近燃着的酒精灯,听声音;步骤⑥的目的是 防止生成的还原铁粉再次被氧化,起保护作用;
(5)若装置D、E分别增重mg和ng,当只有甲烷参与反应时可以求出二氧化碳和水的质量比为9:11,可求m与n的关系;
若缺少装置D,氧元素的测定时取决于B装置的吸收,所以是不会影响的(后面与氧化铁的反应物是甲烷气体反应造成的,所以二氧化碳中的氧元素不会影响到).碳元素的质量分数是通过吸收二氧化碳,也可以说通过E装置的质量增加来实现,当D不存在时,导致部分水被E吸收,而被误当成二氧化碳进行计算,导致碳元素质量增加,进而使含碳量偏大.
(6)装置B中浓硫酸吸收氢气与粗还原铁粉反应生成的水,由该装置增重为反应生成水的质量可求得粗还原铁粉中氧元素质量;装置E中碱石灰吸收甲烷与氧化铁反应产生的二氧化碳,由该装置增重为反应生成二氧化碳的质量可计算出粗还原铁粉中所含碳元素质量.
解答 解:(1)氧化铁在高温条件下能与CO发生反应生成铁与二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)焦炭燃烧放出大量的热,产生的热量使装置内其它反应得以发生;故填:提供热量;
(3)根据题目中的假设情况,为使装置A反应产生的甲烷气体全部在装置C中发生反应,操作时应先将C处酒精灯点燃,然后再点燃A处酒精处;故选④②;故填:④;②;
(4)步骤③的目的是除去装置内的氧气,防止发生爆炸,验证该步骤目的达到的实验方法是收集尾气靠近燃着的酒精灯,听声音;有剩余则没有完全被除掉;步骤⑥的目的是防止生成的还原铁粉再次被氧化,起保护作用;故填:除去装置内的氧气,防止发生爆炸;收集尾气靠近燃着的酒精灯,听声音;防止生成的还原铁粉再次被氧化,起保护作用;
(5)若装置D、E分别增重mg和ng,当只有甲烷参与反应时可以求出二氧化碳和水的质量比为9:11,可求m与n的关系.
3CH4+4Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$8Fe+3CO2+6H2O
3×44 6×18
n m
则列式为$\frac{3×44}{6×18}=\frac{n}{m}$,
则$\frac{n}{m}=\frac{11}{9}$,由于是加热C在前,所以导致会先生成水,导致水的质量多,所以是9n<11m,所以选B.故选B;
若缺少装置D,氧元素的测定时取决于B装置的吸收,所以是不会影响的(后面与氧化铁的反应物是甲烷气体反应造成的,所以二氧化碳中的氧元素不会影响到).碳元素的质量分数是通过吸收二氧化碳,也可以说通过E装置的质量增加来实现,当D不存在时,导致部分水被E吸收,而被误当成二氧化碳进行计算,导致碳元素质量增加,进而使含碳量偏大.故填:不变;偏大;
(6)装置B增重0.180g,则粗还原铁粉与氢气反应生成水的质量为0.180g,生成水中氧元素质量=0.180g×$\frac{16}{18}$×100%=0.160g;样品中氧元素的质量分数=$\frac{0.160g}{10.000g}$×100%=1.6%
装置E增重0.220g,则甲烷与氧化铁反应生成二氧化碳的质量为0.220g,生成二氧化碳中碳元素质量=0.220g×$\frac{12}{44}$×100%=0.060g;样品中碳元素的质量分数$\frac{0.060g}{10.000g}$×100%=0.6%
答:样品中氧和碳元素的质量分数分别为1.6%、0.6%.
故答案为:1.6%;0.6%.
点评 通过对铁冶炼原理的知识迁移,理解该题的实验过程及目的,考查了知识的运用及实验分析的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图所示,上瓶装的是无色的空气,下瓶装的是不与空气发生化学反应的某种红棕色气体,当抽走玻璃片后,过一会,将会发生的现象是红棕色气体逐渐向上瓶中扩散,下瓶颜色变浅,最后上下两瓶中气体的颜色一致,此实验可以说明分子是在不断运动的且分子间存在间隙.
如图所示,上瓶装的是无色的空气,下瓶装的是不与空气发生化学反应的某种红棕色气体,当抽走玻璃片后,过一会,将会发生的现象是红棕色气体逐渐向上瓶中扩散,下瓶颜色变浅,最后上下两瓶中气体的颜色一致,此实验可以说明分子是在不断运动的且分子间存在间隙.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH和MgO的混合物中氧的质量分数为40%,NaOH和MgO的质量一定相等 | |
| B. | 一定量的氯化钠溶液恒温蒸发5克水,析出a克晶体;再蒸发5克水,又析出b克晶体,a与b一定相等 | |
| C. | 用CO完全还原一定质量的FeO,参加反应的CO与通入的CO质量一定相等 | |
| D. | 将98%的浓H2SO4稀释成49%的稀H2SO4,加入水的质量与浓硫酸质量一定相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 48 g | B. | 49 g | C. | 98 g | D. | 99 g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 量筒不仅可以用来量取液体,还可用作反应容器 | |
| B. | 量筒上刻度的最小数值是0,且0mL刻度线在所有刻度线的最上边 | |
| C. | 将量筒放在水平桌面上,右手握试剂瓶,让标签向着手心,慢慢将液体倒入量筒中 | |
| D. | 用10mL量筒量取8.30mL蒸馏水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 若用排空气法收集CO2(密度比空气大)时,气体应从A端通入 | |
| B. | 若用排空气法收集氧气时,气体从B端通入 | |
| C. | 若用排空气法收集H2时,气体应从A端通入 | |
| D. | 若用水将此装置中的O2排出,水应从B端进入 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com